下列描述中,不符合生产实际的是
| A.可用电解饱和MgCl2溶液的方法获得金属镁 |
| B.电解法精炼粗铜,用粗铜作阳极,纯铜作阴极 |
| C.电解熔融Al2O3制备金属铝时,加入冰晶石使Al2O3更易熔化 |
| D.氯碱工业中电解食盐水时,阳离子交换膜可防止氯气与NaOH溶液反应 |
恒温恒压下,在容积可变的器皿中,反应2NO2(气)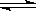 N2O4(气) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
N2O4(气) 达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
| A.不变 | B.增大 | C.减小 | D.无法判断 |
已知:C(s)+CO2(g) 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
| A.升高温度和减小压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
对可逆反应4NH3(g) + 5O2(g) 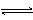 4NO(g) + 6H2O(g),下列叙述正确的是
4NO(g) + 6H2O(g),下列叙述正确的是
| A.达到化学平衡时,5v正(O2)=4v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大 |
| D.达到平衡前,化学反应速率关系:3v正(NH3)=2v正(H2O) |
已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1.则HCN在水溶液中电离的ΔH等于
| A.-67.7 kJ·mol-1 | B.-43.5 kJ·mol-1 |
| C.+43.5 kJ·mol-1 | D.+67.7 kJ·mol-1 |
已知在1×105Pa,298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
| A.H2O(g)=H2(g)+1/2O2(g) ΔH=+242kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-484kJ·mol-1 |
| C.H2(g)+1/2O2(g)=H2O(g) ΔH=+242kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g) ΔH=+484kJ·mol-1 |