下列有关实验装置(装置中略去支撑仪器)进行的相应实验,能达到实验目的的是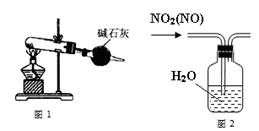

| A.用图1装置以NH4Cl为原料,装置③可用于制备NH3 |
| B.用图2所示装置可除去NO2中的NO |
| C.用图3所示装置比较KMnO4、Cl2、S的氧化性 |
| D.用图4装置制备Fe(OH)2并能较长时间观察其颜色 |
可逆反应:3A(g) 3B(?)+C(?)(ΔH>0),随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( ).
3B(?)+C(?)(ΔH>0),随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是( ).
| A.B和C可能都是固体 |
| B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 |
| D.达平衡时升温,逆反应速率减小 |
将 4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)若经 2 s 后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:
2C(g)若经 2 s 后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:
① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1
③ 2 s时物质 A 的转化率为70%
④ 2 s 时物质 B 的浓度为 0.7 mol·L-1
其中正确的是()。
| A.①③ | B.②③ | C.①④ | D.③④ |
在密闭容器中,NO(g)+CO(g) 1/2N2(g)+CO2(g)△H="-373.2" kJ/mol。达到平衡后,为了提高该反应的速率和NO的转换率,采取的措施正确的是()
1/2N2(g)+CO2(g)△H="-373.2" kJ/mol。达到平衡后,为了提高该反应的速率和NO的转换率,采取的措施正确的是()
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时通入N2 | D.降低温度同时增大压强 |
在密闭容器中进行如下反应:H2(g) +I2(g) 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
| A.T1>T2,ΔH>0 | B.T1>T2,ΔH<0 |
| C.T1<T2,ΔH>0 | D.T1<T2,ΔH<0 |
对于可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)下列叙述正确的是()。
4NO(g)+6H2O(g)下列叙述正确的是()。
| A.达到平衡时:4v正(O2)=5v逆(NO) |
| B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态。 |
| C.达到平衡时,若增加容器容积,则正反应速率减小,逆反应速率增大 |
| D.化学反应的速率关系是:2v正(NH3)=3v逆(H2O) |