氯化铁是一种重要的铁盐,广泛用于造纸、印染等污染处理。
【物质制备】某兴趣小组同学查找到以黄铁矿(主要成分是二硫化亚铁,化学式为FeS2)为主要原料制备氯化铁晶体的工业生产过程: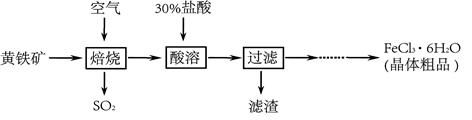
(1)黄铁矿是 物(填“纯净”或“混合”),其中二硫化亚铁中铁元素的化合价为 。
(2)焙烧过程主要发生以下化学反应,配平化学方程式: FeS2 + O2高温Fe2O3 + SO2
(3)该过程产生的尾气中含有HCl等气体,可用 溶液来吸收(填化学式)。
【含量测定】在上述流程中产生的SO2气体可用于工业上生产硫酸,该兴趣小组的同学为测定某黄铁矿中硫元素的含量进行了如下的实验探究。
已知二氧化硫与氢氧化钠反应生成的亚硫酸钠能被过氧化氢氧化成硫酸钠。(假设每步反应均完全,不考虑装置内原有空气对测定结果的影响)
甲、乙二个实验小组均设计了下列装置,称取了m1 g黄铁矿样品,将样品放入如下图所示的硬质粗玻璃管中,从a处不断地缓缓通入空气,高温灼烧玻璃管中的黄铁矿样品至反应完全。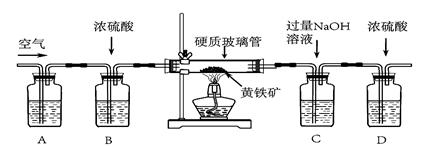
甲组同学仅称量了上述实验所需要的相关装置质量后即完成了测定。
乙组同学则在上述反应结束后,将C瓶中的溶液进行了如下图处理: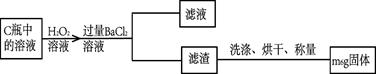
问题讨论:
(4)上述装置中A瓶内所盛的试剂最好是 溶液,其作用是 。
A、B装置能否对调位置? (填“能”或“否”)
(5)气体进入C瓶后,C瓶中发生反应的化学方程式为 。
(6)甲组同学应称量的数据是 (填编号)。
①反应前C装置及其中物质总质量m2 g
②反应前C、D装置及其中物质总质量m3 g
③反应后C装置及其中物质总质量m4 g
④反应后C、D装置及其中物质总质量m5 g
(7)根据(6)中所选数据,甲组同学测得的该黄铁矿中硫元素的质量分数的表达式为 。
(8)乙组同学最终得到的固体的化学式为 ,检验所加BaCl2溶液是否过量的方法是 ,乙组的实验过程中洗涤滤渣的目的是 ,若未洗涤就直接烘干称量,则会使测定结果 (填“偏大、偏小或不变”),检验滤渣是否洗净所用试剂是 溶液,该小组测定的硫元素的质量分数的表达式为 。
用化学符号表示:
(1)钾元素 ;
(2)2个氮原子 ;
(3)3个水分子 ;
(4)+4价的硫元素 ;
(5)镁离子 .
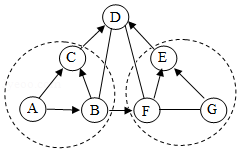
A~G是初中化学常见的物质,B和D能参与光合作用,F可用于改良酸性土壤。 它们之间的关系如图所示(“﹣”表示相连两物质之间能发生反应,“→”表示由某一物成转化为另一物质,部分反应物、生成物及反应条件已略去),每个虚线圈中各反应的基本反应类型相同。
(1)写出物质的化学式:A ,G 。
(2)反应F→E的基本反应类型是 。
(3)反应D﹣F的化学方程式是 。
(4)反应G→E的现象是 。
宏观、微观之间存在必然的联系,建立正确的微粒观有助于化学的学习.请用微粒的知识回答下列问题.
(1)阿伏加德罗指出分子和原子的区别,完善了道尔顿的原子学说.分子和原子的本质区别是 .
(2)“醋酸糖甜”是因为 .
(3)空气和氧气的主要区别是 .
(4)原子内部含有带电荷的质子和电子,而整个原子不显电性的原因是 .
(5)稀盐酸和稀硫酸具有相似的化学性质,原因是 .
金属的研究、利用对于人类社会有着重要意义.
(1)焊锡是锡铅合金,把铅加入锡中制成合金的主要目的是 .
(2)铝制品表面易形成致密氧化铝薄膜,从而阻止铝进一步被空气氧化,但氧化铝能溶于酸.写出氧化铝与稀硫酸反应的化学方程式 .
(3)把装满氯气的集气瓶倒扣于加热至熔化的金属钠上,可观察到的现象是 ,该反应的化学方程式是 .
材料、环境、能源跟生活密切相关.
(1)日常用品尼龙手套、铝壶、不锈钢刀、纯棉桌布中,主要用有机合成材料制成的是 .
(2)为了减小燃烧化石燃料对环境的影响,人们一方面开发利用清洁高效的新能源,
如 (写一种);另一方面提倡“低碳生活”.下列符合“低碳生活”的做法是 (填数字序号).
①人走灯灭 ②少用一次性筷子 ③多使用空调调节温度
(3)目前氢氧燃料电池已经在宇宙飞船等航天器上实际使用,它能把氢气和氧气反应的化学能转化为 能,氢氧燃料电池内反应的化学方程式是 .