芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体。A、B、C、D、E、F和OPA的转化关系如下所示:
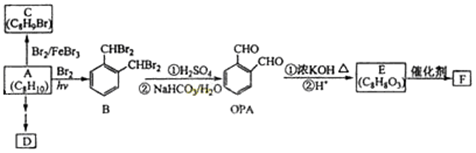
回答下列问题:
(1)A的化学名称是 ;
(2)由A生成B 的反应类型是 。在该反应的副产物中,与B互为同分异构体的化合物的结构简式为 ;
(3)写出C所有可能的结构简式 ;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂。请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用化学方程式表示合成路线 ;
(5)OPA的化学名称是 ,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为 ,该反应的化学方程式为 。(提示 )
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式
用标签如图的浓硫酸配得200 mL某浓度的稀硫酸,现将27.2 g铁粉和氧化铁的混合物加入其中,恰好完全反应,放出氢气2.24 L(标准状况)。反应后的溶液中滴加KSCN不显红色,且无固体剩余物,求:(计算结果保留小数点后1位)
①配制200 mL该稀硫酸,需要浓硫酸 ▲mL;
②混合物中氧化铁的质量为 ▲g;
③稀硫酸的物质的量浓度为 ▲mol·L-1。
有一包白色固体物质,可能含有CuSO4、Na2SO4、KCl、Na2CO3、MgCl2中的一种或几种,现进行如下实验:
(1)将白色固体溶于水中,得到无色透明溶液。
(2)取少量上述溶液两份,其中一份滴加BaCl2溶液,立即产生白色沉淀,再加入稀
硝酸,沉淀没有溶解。另一份溶液中滴加NaOH溶液,有白色沉淀生成。
根据以上实验现象可知,该白色固体中一定含有 ▲,一定没有 ▲,可能有 ▲。
电解铝技术的出现与成熟让铝从皇家珍品变成汽车、轮船、航天航空制造、化工生产等行业的重要材料。工业上用铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)提取纯Al2O3做冶炼铝的原料,某研究性学习小组设计了如下提取流程图
|
|

(1)固体Ⅱ的化学式为_ ▲ ,该固体的颜色为 ▲ ;
(2)在实际工业生产流程⑤中需加入冰晶石,目的是 ▲ ;
(3)写出流程③的离子方程式 ▲ ;
(4)铝粉与氧化铁粉末在引燃条件下常用来焊接钢轨,主要是利用该反应 ▲ ;
(5)从铝土矿中提取铝的过程不涉及的化学反应类型是 ▲ ;
| A.复分解反应 | B.氧化还原反应 | C.置换反应 | D.分解反应 |
(6)生产过程中除NaOH、H2O可以循环使用外,还可以循环使用的物质有_ ▲ _;
(7)若向滤液Ⅰ中逐滴滴入NaOH溶液至过量,产生沉淀随NaOH滴入关系正确的是
Ⅰ溴被称为海洋元素,向盐卤中通入氯气可制得溴:Cl2 + 2NaBr =" 2NaCl" + Br2,该反应被氧化的元素为 ▲(写元素符号);若上述反应制得16g Br2 ,则转移的电子数目是 ▲个。
Ⅱ请按要求书写化学方程式或离子方程式
(1)小明运用化学实验证明了久置于空气中的亚硫酸钠已变质,请用化学方程式表示亚硫酸钠变质的原因 ▲。
(2)FeSO4溶液用稀H2SO4酸化,放置一段时间后略显黄色,写出变化过程的离子方程式 ▲;然后向其中滴加KI-淀粉溶液变蓝色,写出变化过程的离子方程式 ▲_。
A、B、C、D、E、F六种短周期元素,原子序数依次增大。A、E同主族,元素原子的核外电子数是A元素原子核内质子数的两倍。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。D元素原子最外层电子数是次外层电子数的一半。
回答下列问题:
⑴用电子式表示B、F两元素形成化合物的过程:;
⑵A、C两元素的化合物与B的氢氧化物反应的离子方程式为 ;
;
⑶D气态氢化物的稳定性(填“大于”、“小于”)E的气态氢化物的稳定性。