实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表。
| 化合物 |
相对分子质量 |
密度/g·cm-3 |
沸点/℃ |
溶解度/100g水 |
| 正丁醇 |
74 |
0.80 |
118.0 |
9 |
| 冰醋酸 |
60 |
1.045 |
118.1 |
互溶 |
| 乙酸正丁酯 |
116 |
0.882 |
126.1 |
0.7 |
请回答有关问题。
Ⅰ.乙酸正丁酯粗产品的制备
在A中加入11.5mL正丁醇和7.2mL冰醋酸,再加3~4滴浓硫酸,混合均匀,投入沸石。如图所示安装分水器、温度计及回流冷凝管,并在分水器中预先加水至略低于支管口,加热回流,反应一段时间将水逐渐分去,至反应完毕。
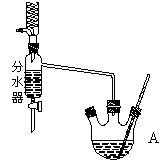
(1)仪器A中发生反应的化学方程式为____________________________。有同学拟通过某种方法鉴定所得产物中是否含有杂质,可采用 确定。
a.红外光谱法 b.1H核磁共振谱法 c.质谱法
(2)“反应中利用分水器将水分去”该操作的目的是: 。
(3)反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是 。
(4)可根据 现象来判断反应完毕。
Ⅱ.乙酸正丁酯粗产品的精制
(5)将仪器A中的液体转入分液漏斗中,用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是 。
(6)再用10ml 10% Na2CO3溶液洗涤有机层,该步操作的目的是 。
(7)将干燥后的产品蒸馏收集乙酸正丁酯产品时,应将温度控制在 左右。
(13分)重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下: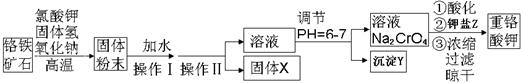
试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有。铁在周期表的位置是。
(2)操作Ⅱ的名称是。
(3)固体X的主要成分是___________,沉淀Y的主要成分是。
(4)流程中①酸化所用的酸和②钾盐Z最合适的是(填符号)________,
| A.盐酸和氯化钾 | B.硫酸和氯化钾 |
| C.硫酸和硫酸钾 | D.次氯酸和次氯酸钾 |
酸化反应的离子方程式为。
(5)FeO·Cr2O3与氯酸钾、氢氧化钠高温反应化学方程式:。
(14分)某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此实验小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
已知:常温下,CO能使一些化合物中的金属离子还原。例如:PdCl2+CO+H2O=Pd↓+CO2+2HCl,反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。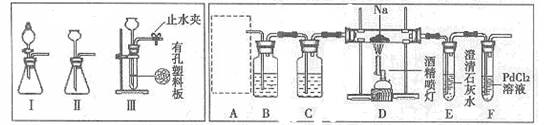
请回答下列问题:
(1)为了使制气装置能“随开随用,随关随停”,上图A处制取CO2气体应选用的装置是(填写“I”、“II”或“III”),其离子方程式是。装置B和C中应盛放的试剂分别是,。
(2)观察实验装置图可知Na与CO2反应的条件是,检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是,这步操作的目的是。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是。
(4)请判断②中D装置生成固体的成分是钠的(填“正盐”或“酸式盐”)。请用文字简要说明理由。
三草酸合铁酸钾晶体易溶于水,难溶于乙醇,可用作某些化学反应的催化剂,化学式为K3[Fe(C2O4)3]·3H2O。实验室以铁屑为原料制备三草酸合铁酸钾晶体相关反应过程如图所示:
请回答下列问题:
(1)制备过程中加入H2O2目的是______________,得到K3[Fe(C2O4)3]溶液后,需要加入乙醇,其目的是_________________。
(2)晶体中所含的结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复脱水、冷却、称量至恒重,⑥计算。步骤⑤的目的是___________________。
(3) 可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
①写出滴定过程中发生反应的离子方程式_____________;
②取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用0.1mol·L-1的酸性高锰酸钾溶液进行滴定,达到滴定终点时消耗酸性高锰酸钾溶液24mL。则产物中K3[Fe(C2O4)3]·3H2O的质量分数为_________。(K3[Fe(C2O4)3]·3H2O相对分子质量为491)
亚硝酸钠在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示(部分夹持装置略)。
已知:
①3NaNO2+3HCl 3NaCl+HNO3+2NO↑+H2O
3NaCl+HNO3+2NO↑+H2O
②酸性条件下,NO或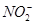 都能与
都能与 反应生成
反应生成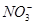 和Mn2+;
和Mn2+;
完成下列填空:
(1)写出a仪器的名称________________。
(2)为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为_________________。
(3)写出NO与Na2O2在常温下生成NaNO2的化学反应方程式______________;当该反应中转移0.1mol e-时,理论上吸收标准状况下NO的体积为___________L。
(4)D装置中发生反应的离子方程式为_____________________。
(5)将11.7g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭_____________g。
某NiO的废料中有FeO、CuO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4和Ni的流程如下:
已知:有关金属离子生成氢氧化物沉淀所需的pH如下图:
(1)滤渣1的主要成分为。
(2)电解脱铜:金属铜在极析出。
(3)①用离子方程式解释加入H2O2的作用。
②加Na2CO3调节溶液的pH至5,则滤渣2的主要成分为。
(4)从滤液2中获得NiSO4.6H2O的实验操作是、过滤、洗涤、干燥。
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理示意图如下:
①A极的电极反应式为和2H++2e-=H2↑。
②B极附近pH会(填“增大”、“减小”或“不变”);用平衡移动原理解释B极附近pH变化的原因:。
③若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),理论上能得到Nig。