1,2-二溴乙烷可做抗爆剂的添加剂,常温下为无色液体,密度为2.18g cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题:
cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题:

(1)写出制备1,2—二溴乙烷的两个反应方程式:
______________________________________、 。
(2)安全瓶b可以防止倒吸,并用于检查实验进行时试管d是否发生堵塞,请写出发生堵塞时b的现象: _________________________________________。
(3)容器c中NaOH溶液的作用是:__________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出很多。如果装置的气密性没有问题,试分析其可能的原因 。
(5)e装置内NaOH溶液的作用是:__________________________________。
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3;乙同学认为沉淀可能是Cu(OH)2;丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均 不带结晶水)
不带结晶水)
Ⅰ.按照甲同学的观点,发生反应的离子反应方程式为;
在探究沉淀成分前,须将沉淀从溶液中分离并净化。其具体操作依次为、、。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。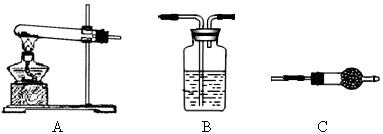
(1)各装置连接顺序为→→。
(2)能证明生成物中有CuCO3的实验现象是。
Ⅲ.若CuCO3和Cu(OH)2两者都有,可利用下列装置通过实验测定其组成。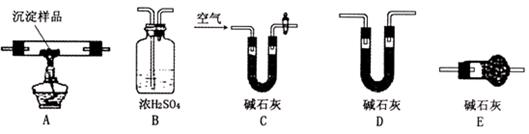

(1)装置C中碱石灰的作用是,实验开始和结束时都要通入过量的空气,请说明结束时通入过量空气的作用是
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为。
某化学兴趣小组用下图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。
⑴写出该实验中生成乙烯的化学方程式:
⑵甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是(填字母序号)
A、乙烯与溴水易发生取代反应
B、使溴水褪色的反应,未必是加成反应
C、使溴水褪色的物质,未必是乙烯
D、浓硫酸氧化乙醇生成乙醛,也会使溴水褪色
⑶乙同学经过细致观察后认为试管中另一现象可证明反应中有乙烯生成,这个现象是
⑷丙同学对上述实验装置进行了改进,在I和II之间增加如图装置,则A中的试剂应为,其作用是,B中的试剂为。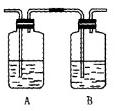
⑸处理上述实验后烧瓶中废液的正确方法是(填字母序号)。
A、废液冷却后倒入下水道中
B、废液冷却后倒入空废液缸中
C、将水加入烧瓶中稀释后倒入废液缸
电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量:(1)若用下列仪器和导管组装实验装置:
(1)如果所制气体流向从左向右时,上述仪器和导管从从上到下,从左到右直接连接的顺序(填各仪器,导管的序号)是接接接接接。
(2)碳化钙和水反应的化学方程式
某课外小组设计的实验室制取乙酸乙酯的 装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
装置如图14-2所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。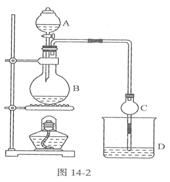
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6 C2H50H
②有关有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点/℃ |
34.7 |
78.5 |
118 |
77.1 |
请回答:
(1)浓硫酸的作用是;若用同位素180示踪法确定反应产物水分子
中氧原子的提供者,写出能表示180位置的化学方程式:
。
(2)球形干燥管C的作用是。若反应前向D中加入几滴酚酞,现象:;反应结束后D中的现象是.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出;再加入(此空从下列选项中选择),然后进行蒸馏,收集77℃左右的馏分,以得较纯净的乙酸乙酯。
| A.五氧化二磷 | B.碱石灰 | C.无水硫酸钠 | D.生石灰 |
某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上步骤有错误的是(填编号),该错误操作会导致测定结果
(填“偏大”、“偏小”或“无影响”)__________________
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,测定结果(填“偏大”、“偏小”或“无影响”)___________________
(3)判断滴定终点的现象是:
(4)下图是某次滴定时的滴定管中的液面,其读数为mL