实验室制乙烯,常常因为温度过高而使乙醇与浓硫酸反应生成少量的二氧化碳,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
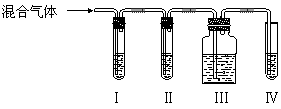
(1)写出实验室制取乙烯的化学方程式________________________________
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中可盛放的试剂是:(将下列有关试剂的序号填入空格内)
Ⅰ: 、Ⅱ: 、Ⅲ: 、Ⅳ: 。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
(3)能说明二氧硫存在的现象是 。
(4)使用装置(Ⅱ)的目的是 。
(5)使用装置(Ⅲ)的目的是 。
(6)确证含乙烯的现象 。
(7)进行下列实验时,都要使用温度计,回答下列问题:
制取乙烯时,温度计水银球部位应放在 。
石油分馏时,温度计水银球部位应放在 。
结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是 (填字母)。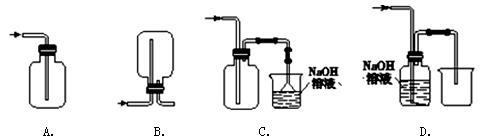
(2)漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为 。
漂白粉与浓盐酸发生氧化还原反应,化学方程式为 。
(3)实验室可以用MnO2和浓盐酸在加热条件下制备Cl2,还可以用KMnO4与浓盐酸在常温下制备Cl2。高锰酸钾溶液常用于物质的定性检验与定量分析。某化学兴趣小组在实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol/L的KMnO4溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、 。
②下列操作会导致实验结果偏小的是 (填字母)。
a.加水定容时俯视刻度线
b.容量瓶内壁附有水珠而未干燥处理
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
(4)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。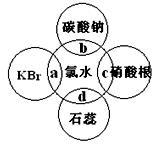
①能证明氯水具有漂白性的是__________(填“a”、“b”、“c”或“d”)。
②c过程中的现象是___________________。
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的浓度, 请填写下列空白:
(1)将10.00 mL过氧化氢溶液移至250mL (填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数分别填在下列横线和括号内。
MnO4- + H2O2 + H+ = Mn2+ + O2 + H2O
(3)KMnO4标准液装在 滴定管,滴定到达终点的现象是
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的浓度为
(5)若盛装高锰酸钾标准溶液的滴定管用蒸馏水洗后没有用标准液润洗,则测定结果 (填“偏高”或“偏低”或“不变”)。
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的化学方程式如下:
2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用下图装置A制取氨气,你所选择的试剂是。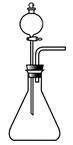
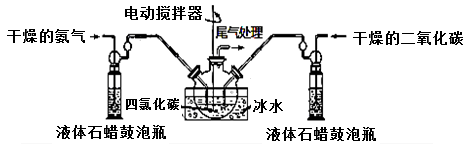
装置A装置B
(2)制备氨基甲酸铵的装置B如上图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是: 、 。液体石蜡鼓泡瓶的作用是: 。
②从反应后的混合物中分离出产品,为了得到干燥产品,应采取的方法是_______(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
③尾气处理装置如图所示。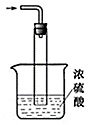
双通玻璃管的作用:;浓硫酸的作用: 、 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品11.73 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为15.00 g。
则样品中氨基甲酸铵的物质的量分数为 _____ 。
某地区的雾霾中含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。
收集该地区的雾霾,经必要的预处理后得试样溶液,取适量该试样溶液进行如下实验:
已知:3NO3-+ 8Al + 5OH-+ 2H2O 3NH3+ 8AlO2-
3NH3+ 8AlO2-
根据以上实验操作与现象,回答下列问题:
(1)气体X的分子式为________________;沉淀1的主要成分是 (填化学式)。
(2)生成沉淀2的离子方程式有两个,分别是 ___、 。
(3)第④步发生反应,每产生5.6 L标准 状况下的气体X,转移电子的物质的量为 。
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:该实验的主要操作步骤如下:
①配制100mL 1.0mol•L﹣1的盐酸溶液;
②用 (填仪器名称并注明规格)量取7.5mL 1.0mol•L﹣1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为 g;
④往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL.
请将上述步骤补充完整并回答下列问题.
(1)步骤①中,配制100mL 1.0mol•L﹣1的盐酸溶液时,下列哪些操作会使配制浓度偏小 (填写字母).
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线,继续加水至刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤② ,步骤③ g.
(3)实验步骤⑤中应选用 (填字母)的量筒.
A.100mL B.200mL C.500mL
(4)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm= L/mol.
(5)若未除去镁条表面的氧化膜,则测得该条件下气体的摩尔体积 (填偏大、偏小或无影响).