一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH – 4e- + H2O = CH3COOH + 4H+。下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e- + 2H2O = 4OH- |
在一定条件下,在密闭容器中反应:2NO2(g)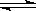 O2(g)+ 2NO(g) ΔH>0,达到
O2(g)+ 2NO(g) ΔH>0,达到 平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
平衡。当改变其中一个条件X,Y随X的变化符合图中曲线的是
| A.当X表示温度时,Y表示NO的物质的量 |
| B.当X表示压强时,Y表示NO2的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示。下列说法正确的是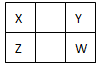
| A.Z元素的原子半径可能比Y元素的小 |
| B.Z的最高价氧化物的水化物的酸性一定比W的强 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z元素的最高化合价可能比Y元素的高 |
下述实验中,不能达到预期目的的是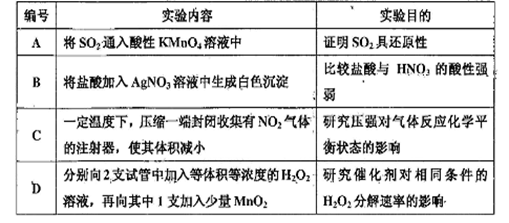
下列离子方程式的书写正确的是
| A.向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+=SO2↑+H2O |
| B.玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-=Na2SiO3↓+H2O |
| C.高锰酸钾酸性溶液吸收二氧化硫:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ |
| D.Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O |
金属铜与人体分泌物中的盐酸以及子宫内的空气反应可生成超氧酸:Cu+HCl+O2=Cu Cl+HO2 HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
Cl+HO2 HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是
A. 氧化剂 氧化剂 是O2 是O2 |
B.HO2在碱中能稳定存在 |
| C.氧化产物是HO2 | D.1 mol Cu参加反应有2 mol电子发生转移 |