过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:____________。
(2)Na2O2,K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。则上述最适合的过氧化物是________。
(3)甲酸钙[ (HCOO)2 Ca]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛溶液依次加入到质量分数为30%-70%的过氧化氢溶液中,则该反应的化学方程式为________。过氧化氢比理论用量稍多,其目的是________。反应温度最好控制在30 -70℃,温度不易过高,其主要原因是________。
(4)下图是硼氢化钠一过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH_____(填“增大”、
“减小”或“不变”)。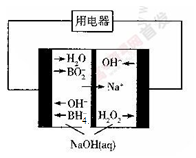
(5)研究CO2的利用对促进低碳社会的构建具有重要意义。250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2 (g)+CH4(g)  2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物 质 |
CH4 |
CO2 |
CO |
H2 |
| 体积分数 |
0.1 |
0.1 |
0.4 |
0.4 |
①此温度下该反应的平衡常数K=__________
②已知:CH4(g)+2O2(g) ===CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1
CO(g)+H2O (g) ===CO2(g)+H2 (g) △H="+2.8" kJ·mol-1
2CO(g)+O2(g) ===2CO2(g) △H=-566.0 kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H=________________
2CO(g)+2H2(g) 的△H=________________
近几年开发的甲醇燃料电池是采用铂作电极催化剂,电池中的质子交换膜只允许质子和水分子通过。其工作原理的示意图如下: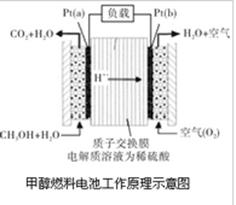
请回答下列问题:
(1)Pt(a)电极对应发生的电极反应为。Pt(b)电极反生反应(填“氧化”或“还原”),电极反应为。
(2)电池的总反应方程式为。
(3)如果该电池工作时电路中通过2mol电子,则消耗的CH3OH有mol。
如图I是广州亚运会开幕式“红棉花开迎宾来”焰火盛宴的一个场景,请回答下列问题:
(1)焰火利用了部分金属的元素特征的()反应。
(2)现在有一种火焰的引发是当浓H2SO4滴下去跟氯酸钾起作用时,便生成了其臭的二氧化氯气体,且发现只有氯元素的化合价发生变化,请写出该反应的方程式。
(3)如图2所示的五元环代表A,B,C,D,E五种物质,圆圈交叉部分指两种化合物含有一种相同元素,五种物质有五种短周期元素组成,每种化合物仅含两种元素,A是沼气的主要成分,B,E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液时医疗上广泛使用的消毒剂,E的分子结构模型为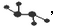 C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数比为3:2.根据上信息回答下列问题:
C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数比为3:2.根据上信息回答下列问题:
①D的化学式是;
②B的电子式是;
③C与纯碱反应的化学方程式为。
某小组学生想研究不同物质对双氧水分解速率的影响,以生成气体量50mL为标准,设计了如下实验方案:
| 实验序号 |
双氧水体积 |
双氧水浓度 |
添加的物质 |
待测数据X |
| 1 |
100mL |
20% |
无 |
|
| 2 |
100mL |
20% |
10gMnO2 |
|
| 3 |
100mL |
20% |
10gKI |
|
| 4 |
100mL |
20% |
新鲜猪肝 |
(1)在该研究方案中,MnO2、KI和猪肝在双氧水分解的过程中可能起到的作用。
(2)待测数据X为。
(3)以下措施可以加快该实验中双氧水分解速率的是:(填标号)。
A.将双氧水的体积增大至200mL
B.将双氧水的浓度增大至30%
C.对装置A加热
D.上下移动B装置使量气管内气体压强增大
(4)从控制变量的原理来看,该方案是否合理(填“是”或“否”)。理由是:
(9分)盐酸常用于清除金属表面的铜锈铁锈。某同学欲将除锈后的盐酸中的金属元素分步沉淀,查资料获知常温下水溶液中各离子沉淀的pH范围:
| 离子 |
开始沉淀的pH |
沉淀完全的pH |
| Fe3+ |
1. 0 |
3. 0 |
| Fe2+ |
5. 8 |
8. 8 |
| Cu2+ |
4.2 |
6.7 |
(1)若以离子浓度降至1×10-5 mol·L-1为沉淀完全,根据上表数据推算出ksp[Fe(OH)3]=
(2)根据上述数据该同学设计了以下实验流程:
A可能是;试剂B的化学式是;沉淀②化学式是。
(8分)84消毒液是一种以次氯酸钠为主要成分的高效消毒剂。
(1)次氯酸钠溶液呈碱性,原因可用离子方程式表示为;
(2)二氧化碳、氢氧化钠、氯化钠三种物质中,添加到84消毒液中可增强其消毒效果的是;
(3)84消毒液可以通过电解氯化钠稀溶液制取,电解装置通常选用铁和碳棒为电极,电解时铁电极反应式为。