空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)溴在周期表中位于_________周期,_________族。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,为什么? 。
(3)步骤④的离子方程式: __________________________ 。
(4)步骤⑥的蒸馏过程中,溴出口温度为何要控制在80—900C。温度过高或过低都不利于
生产,请解释原因__________________________________________ 。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是_____________,分离时液溴从分离器的_____(填“上口”或“下口”)排出。
(6)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”___ 。
某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的一种或几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:
(1)溶液中一定含有的溶质是 ,一定不含有的溶质是 (填化学式)。
(2)溶液中可能含有的溶质是 (填名称),判断该物质是否存在的实验方法是 ,现象是 。
(3)分别写出AB段、BC段发生反应的离子方程式:
①AB段为 ;
②BC段为 。
下图所示是从铝土矿(主要成分是Al2O3,含Fe2O3、SiO2等杂质)中提取氧化铝的工艺流程之一。
已知:SiO2能和氢氧化钠反应,不和盐酸反应。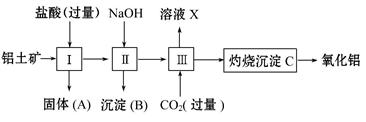
回答下列问题:
(1)用盐酸溶解铝土矿后,所得溶液中的阳离子有 。
(2)固体A的主要成分是 。
(3)进行操作Ⅱ时,为了达到分离要求,加入的NaOH应该 。
(4)进行操作Ⅲ时,一般通入过量CO2,其反应的化学方程式是
。
(5)溶液X和盐酸反应的离子方程式为
。
含镁3%~5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:
镁铝合金 溶液
溶液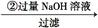 得到沉淀的质量为m2g;
得到沉淀的质量为m2g;
实验设计2:
镁铝合金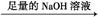 生成的气体在标准状况下的体积为V1L。
生成的气体在标准状况下的体积为V1L。
实验设计3:
镁铝合金 生成的气体在标准状况下的体积为V2L。
生成的气体在标准状况下的体积为V2L。
请回答以下问题:
(1)写出实验设计1中单质铝在第①步中发生反应的离子方程式:
。
(2)写出实验设计2中反应的离子方程式: 。
(3)判断这几种实验设计能否求出镁的质量分数,能求出的用题目提供的数据将镁的质量分数表示出来,不能求出的就空着不填。
①实验设计1: 。
②实验设计2: 。
③实验设计3: 。
某无色溶液中只含有下列8种离子中的某几种:Mg2+、H+、Ag+、Na+、Cl-、HC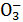 、OH-、N
、OH-、N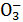 ,已知该溶液能与铝反应放出氢气。试回答下列问题:
,已知该溶液能与铝反应放出氢气。试回答下列问题:
(1)若反应后生成Al3+,则溶液中可能存在的离子有 ,一定存在的离子有 ,一定不存在的离子有 ,反应的离子方程式为 。
(2)若反应后生成Al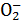 ,则溶液中可能存在的离子有 ,一定存在的离子有 ,一定不存在的离子有 ,反应的离子方程式为 。
,则溶液中可能存在的离子有 ,一定存在的离子有 ,一定不存在的离子有 ,反应的离子方程式为 。
金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下: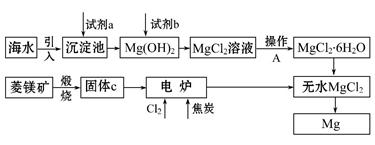
回答下列问题:
(1)试剂a的化学式是 。
(2)加入试剂b发生反应的离子方程式是
。
(3)操作A是蒸发浓缩、冷却结晶、 。
(4)在电炉中参加反应的n(Cl2)∶n(焦炭)=1∶1,则该反应的化学方程式是
。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是(写出一种即可)
。