含镁3%~5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料。现有一块已知质量为m1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:
镁铝合金 溶液
溶液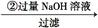 得到沉淀的质量为m2g;
得到沉淀的质量为m2g;
实验设计2:
镁铝合金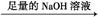 生成的气体在标准状况下的体积为V1L。
生成的气体在标准状况下的体积为V1L。
实验设计3:
镁铝合金 生成的气体在标准状况下的体积为V2L。
生成的气体在标准状况下的体积为V2L。
请回答以下问题:
(1)写出实验设计1中单质铝在第①步中发生反应的离子方程式:
。
(2)写出实验设计2中反应的离子方程式: 。
(3)判断这几种实验设计能否求出镁的质量分数,能求出的用题目提供的数据将镁的质量分数表示出来,不能求出的就空着不填。
①实验设计1: 。
②实验设计2: 。
③实验设计3: 。
右边图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色反应均为黄色。
请填写下列空白: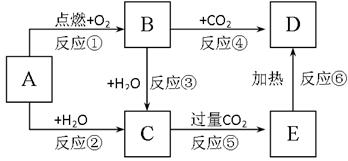
(1)写出化学式:
A 、B、
C 、D 。
(2)以上反应中属于氧化还原反应的有。(填写编号)
(3)写出A → C反应的离子方程式;
E → D的化学方程式。
将500mL0.1mol/L的CuSO4溶液和500mL4mol/L的NaCl溶液相混合,然后用石墨电极进行电解,电解过程中共有0.4mol电子通过。试计算:
(1)阴极上可析出铜克。
(2)在标准状况下阳极上可以产生毫升气体。
(3)假设电解过程中溶液体积的变化忽略不计,则当有0.2 mol电子通过时,溶液的PH为。
已知,当羟基与双键碳原子相连接时,易发生如下转化: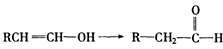 化学式为C8H8O2的有机物有如下的转化关系:
化学式为C8H8O2的有机物有如下的转化关系: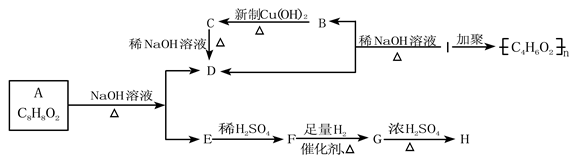
其中F能与FeCl3溶液显紫色,I为一种不饱和酯。
回答:
(1)结构简式E,B,I。
(2)写出反应类型:B→C; G→H。
(3)写出下列反应的化学方程式
①A→D+E。
②B→C。
(4)写出与A具有相同官能团、且属于芳香族化合物的同分异构体的结构简式(不含A):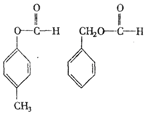
、、。
某无色溶液可能是由Na2CO3、 NaOH 、MgCl2、AlCl3、BaCl2 、Fe2(SO4)3 、(NH4)2SO4溶液中的两种或两种以上混合而成。取该溶液少许于试管,向其中加入H2SO4,有白色沉淀生成,继续加入H2SO4时沉淀又完全消失,整个实验过程中无气体产生,则原溶液是由和混合而成。实验过程中有关的离子反应方程式是
有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E
的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2
反应生成C2A和气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称:A_______,B_______, E_______。
(2)画出E的原子结构示意图_______。
写出电子式D2A2_______,EB4_______。
(3)比较EA2与EB4的熔点高低(填化学式)_______>_______。
(4)A的氢化物的沸点与同族下一周期元素的氢化物相比,A的氢化物的沸点(填“高”或“低”),原因是。