X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相 关 信 息 |
| X |
X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y |
Y是地壳中含量最高的元素 |
| Z |
Z的基态原子最外层电子排布式为3s23p1 |
| W |
W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第 周期第 族;W的原子半径比X的 (填“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是 ;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是 ;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
(4)在25℃、101Kpa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419KJ,该反应的热化学方程式是 。
某工厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红(Fe2O3)和氧化铜。(已知铜能溶解在稀硝酸中生成硝酸铜溶液)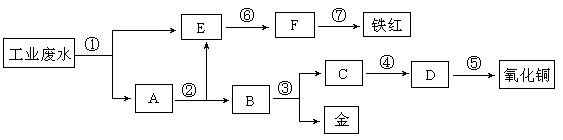
请填写下面空白:
(1)图中标号处需加入的相应物质分别是(填化学式)①②
③④;
(2)A处固体成分为(填化学式)
(3)写出⑤处反应的化学方程式;
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)该浓硫酸的物质的量浓度为__________mol/L。
(2)取用任意体积的该硫酸溶液时,下列物理量中不随所取体积的多少而变化的是__________。
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液中SO42-的数目 D.溶液的密度
(3)某学生欲用上述浓硫酸和蒸馏水配制480 mL物质的量浓度为0.2 mol/L稀硫酸。
①该学生需要量取________mL上述浓硫酸进行配制。
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________________;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓硫酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的硫酸沿玻璃棒注入一定体积的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
③在配制过程中,下列实验操作使所配制的稀硫酸的物质的量浓度偏高的是_________
A.用量筒量取浓硫酸时仰视观察凹液面
B.稀释用的烧杯和玻璃棒未洗涤
C.洗净的容量瓶未经干燥就用于配制溶液
D.溶液注入容量瓶前没有恢复到室温就进行定容
E.定容时俯视观察凹液面
F.加水超过刻度线后,用胶头滴管吸出多余的液体
④现将100mL该硫酸与300mL 0.4mol/LCuSO4溶液混合,体积变化忽略不计,所得溶液中SO42-的物质的量浓度是_________mol/L。
铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。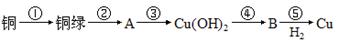
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?___________________________。
(2)请写出②处的离子方程式。______________________________________________________________,
(3)上述转化过程中属于氧化还原反应的是_________(填序号,下同),属于复分解反应的是__________。
⑴下列物质:①熔融氯化钠②盐酸③纯醋酸(CH3COOH)④碳酸钙 ⑤酒精 ⑥二氧化碳 ⑦硫酸氢钠固体⑧铜 ⑨碳酸氢钠固体⑩氢氧化钡溶液,属于电解质的是, 属于非电解质的是,能导电的是。(用序号填空)
⑵写出物质③和⑨在水中反应的离子方程式:。
⑶将物质⑦配制成溶液,逐滴滴入⑩中至Ba2+恰好沉淀完全,写出离子方程式:。
设反应①Fe(s)+CO2(g) FeO(s)+CO(g)△H=Q1的平衡常数为K1,
FeO(s)+CO(g)△H=Q1的平衡常数为K1,
反应②Fe(s)+H2O(g) FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g)△H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度(T) |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是________(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g)△H=Q3
CO(g)+H2O(g)△H=Q3
①根据反应①与②推导出K1、K2、K3的关系式K3=_____________;可推断反应③是________(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有__________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂
D.设法减少CO的量E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3=_____________;