某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:
mCeO2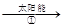 (m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2
(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+xH2O+ xCO2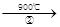 mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
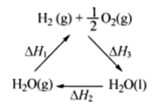
下列说法不正确的是
| A.该过程中CeO2没有消耗 |
| B.该过程实现了太阳能向化学能的转化 |
| C.上图中△H1=△H2+△H3 |
| D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O |
下列有机物中,所有原子可能处于同一平面的是
| A.乙烷 | B.甲苯 | C.丙炔 | D.苯乙烯 |
既能使FeCl3溶液显色,又能和NaHCO3溶液放出气体的有机物是
下列有机物的命名正确的是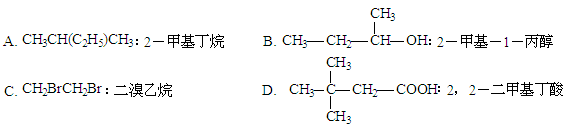
下列各组物质中,一定互为同系物的一组是
| A.C3H6与C5H10 | B.C3H8与C5H12 |
| C.分子式为CH4O和C2H6O的物质 | D.苯酚和苯甲醇(C6H5CH2OH) |
下列叙述:①中国科学家于1965年首次人工合成了具有生物活性的蛋白质——结晶牛胰岛素;②瑞典化学家贝采利乌斯首次提出了“有机化学”的概念;③德国化学家维勒首次人工合成了有机物——尿素;④德国化学家李比希首创了有机物的定量分法方法和“基团”理论。其中正确的是
| A.① | B.①③ | C.①②③ | D.①②③④ |