氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时
①HF(aq)+OH—(aq)=F—(aq)+H2O(l) △H=—67.7KJ·mol—1
②H+(aq)+OH—(aq)=H2O(l) △H=—57.3KJ·mol—1
在20mL0.1·molL—1氢氟酸中加入VmL0.1mol·L—1NaOH溶液,下列有关说法正确的是
| A.氢氟酸的电离方程式及热效应可表示为HF(aq)=H+(aq) +F−(aq)△H=+10.4KJ·mol—1 |
| B.当V=20时,溶液中:c(OH—)=c(HF) +c(H+) |
| C.当V=20时,溶液中:c(F—)<c(Na+)=0.1mol·L—1 |
| D.当V>0时,溶液中一定存在:c(Na+)>c(F—)>c(OH—)>c(H+) |
向10.00 mL 0.01 mol/L某一元酸HA溶液中逐滴加入0.01 mol/L NaOH 溶液,溶液pH变化曲线如右图所示。下列说法不正确的是( )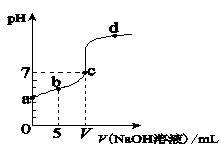
A.HA是弱酸
B.b点表示的溶液中:2c(Na+) = c(A-) + c(HA)
C.c点时:V=" 10.00" mL
D.b、c、d点表示的溶液中:c(Na+) + c(H+) = c(A-) + c(OH-)
在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊的NH4Cl溶液②滴有石蕊的CO2溶液
③滴有石蕊的H2SO4溶液④滴有酚酞的氨水溶液
⑤滴有酚酞的氢氧化钠溶液⑥滴有酚酞的饱和氢氧化钙溶液
⑦滴有酚酞的Na2CO3溶液⑧ 溶有SO2的品红溶液
| A.②④ | B.①③⑤⑦ | C.①④⑥⑧ | D.②④⑥ |
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是( )
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,可脱去2mol Cl2 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
NH3中氢原子可被锂原子替代。亚氨基锂(Li2NH)是一种良好的固体储氢材料,其储氢原理可表示为:Li2NH+H2→LiNH2+LiH。下列有关说法正确的是( )
| A.Li2NH中N的化合价为-1 |
| B.此法储氢和钢瓶储氢的原理相同 |
| C.LiH中的阳离子半径大于阴离子半径 |
| D.该反应中H2既是氧化剂又是还原剂 |
下列各项内容中,排列顺序正确的是( )
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②相同物质的量浓度的下列溶液中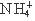 的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
的浓度:(NH4)2SO4>(NH4)2CO3>NH4Cl
③微粒半径:K+>S2->F-
④给出质子的能力:CH3COOH>C2H5OH>H2O
⑤氢化物的沸点:H2Se>H2S>H2O
| A.①③ | B.②④ | C.①② | D.③⑤ |