硫酸钠-过氧化氢加合物(xNa2SO4 ·yH2O2 ·zH2O)的组成可通过下列实验测定:①准确称取1. 7700 g 样品,配制成100. 00 mL 溶液A。②准确量取25. 00 mL 溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0. 5825 g。③准确量取25. 00 mL 溶液A,加适量稀硫酸酸化后,用0. 02000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液25. 00 mL。H2O2与KMnO4反应的离子方程式如下:2MnO4- +5H2O2+6H+=2Mn2++8H2O+5O2↑
(1)已知室温下BaSO4的Ksp ="1." 1伊10-10,欲使溶液中c(SO42-)≤1. 0×10-6 mol·L-1,应保持溶液中c(Ba2+)≥ mol·L-1。
(2)上述滴定若不加稀硫酸酸化,MnO4- 被还原为MnO2,其离子方程式为 。
(3)通过计算确定样品的组成(写出计算过程)。
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为:。 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4g和13.2g。 |
(2)A的分子式 为:。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团:。 |
(4)A的核磁共振氢谱如下图: |
(4)A中含有种氢原子。 |
| (5)综上所述,A的结构简式。 |
五种有机物A、B、C、D、E,其中A、B是烃类,其它为含氧衍生物;A与E、B与D分别碳数相同。常温常压下A为气体,B、C是液体,D为固体。已知:
(1)A可以聚合;完全燃烧1molA,需氧气3mol。
(2)B的蒸气对氢气的相对密度是39,完全燃烧7.8g B,需氧气16.8L(标准状态)。
(3)C与浓硫酸共热得A,C经氧化可得E。
(4)D溶液遇FeCl3溶液显紫色,E与Na2 CO3溶液混和有气体产生。
CO3溶液混和有气体产生。
由上述推断出各物质的结构简式:
A._________、B.___________、C.__________、 D.___________、E.____________。
(1)卤代烃的用途十分广泛。卤代烃(填“能”或“不能”)跟硝酸银溶液反应生成卤化银沉淀。分子式为C3H7Br的卤代烃,其结构简式有两种,分别为
和,它们与NaOH醇溶液反应生成的有机物的结构简式为。为了检验这 种有机物,可把它通入盛有的试管中。
种有机物,可把它通入盛有的试管中。
(2)分子式为C4H10O,属于醇的同分异构体有种,其中一种不能氧化成醛或酮,它的结构简式是;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式。
命名下列物质或根据题意写出结构简式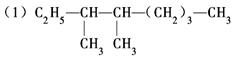 的系统命名法名称是。
的系统命名法名称是。
⑵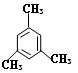 的名称是。
的名称是。
(3) 2-甲基-1-丁烯的结构简式 ,
,
(4) 相对分子质量为72且沸点最低的烷烃的结构简式。
(1)在9.5g某二价金属的氯化物中含0.2mol Cl—,此氯化物的摩尔质量为;该金属元素的相对原子质量为。
(2) 已知N2、CO2的混合气体的质量共10.0克,标准状况下,体积为6.72L,原混合气体中N2、CO2的体积之比.