下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是
| A.气态氢化物的稳定性为H2T<H2R |
| B.单质与稀盐酸反应的速率为L<Q |
| C.M与T形成的化合物具有两性 |
| D.L2+与R2-的核外电子数相等 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A.CO2的电子式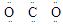 |
B.Cl-的结构示意图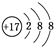 |
C.氨分子的球棍模型: |
D.质量数为37的氯原子Cl |
国家核事故应急协调委员会2011年4月4日权威发布:我国内地31个省、自治区、直辖市部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素131I。下列有关说法正确的是
| A.131I与127I互为同素异形体。 | B.131I比127I多4个质子 |
| C.131I与127I是同一核素 | D.131I与127I互为同位素 |
不需要在棕色瓶中存放的物质是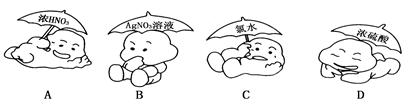
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银)︰n(硝酸亚汞)=2︰1,则下列表述正确的是
A在两个阴极上得到的银和汞的物质的量之比n(银)︰n(汞)=2︰1
B在两个阳极上得到的产物的物质的量不相等
C硝酸亚汞的分子式为HgNO3
D硝酸亚汞的分子式为Hg2(NO3)2
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:CH2=CH2(g) + H2O(g) CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是
CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等。下图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是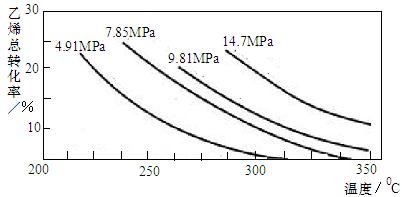
| A.合成乙醇的反应一定为吸热反应 |
| B.目前工业上采用250~300℃,主要是在此温度下乙烯的转化率最大 |
| C.目前工业上采用加压条件(7MPa左右),目的是提高乙醇的产率和加快反应速率 |
| D.相同催化剂下,在300℃ 14.7MPa乙醇产率反而比300℃ 7MPa低得多,是因为加压平衡向逆反应方向移动 |