下列有关实验原理、操作及安全知识的叙述,正确的是
| A.不慎将苯酚固体粉末沾在皮肤上,立即用大量热水(>65℃)冲洗 |
| B.在用标准盐酸滴定未知浓度NaOH溶液时,滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失,会使测定结果偏低 |
| C.把玻璃管插入橡胶塞孔时,可用厚布护手,紧握用水湿润的玻管,缓慢旋进塞孔中 |
| D.银氨溶液、Cu(OH)2悬浊液、硫酸溶液、氯水在实验室里均不宜长期放置 |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的的是( )
A.甲烷、CO合成乙酸乙酯:2CH4+2CO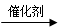 CH3COOCH2CH3 CH3COOCH2CH3 |
B.烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+ H2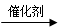 RCH2CH2CHO RCH2CH2CHO |
C.甲烷与氯气反应制氯仿:CH4+3Cl2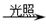 CHCl3+3HCl CHCl3+3HCl |
| D.乙烯合成聚乙烯 |
化学与环境、材料和科技等密切相关。下列说法中错误的是()
| A.积极推行“限塑令”,加快研发利用二氧化碳合成的聚碳酸酯类可降解塑料 |
| B.光导纤维在信息产业中有广泛应用,制造光导纤维的主要材料是单质硅 |
| C.即将到来的新能源时代,核能、太阳能和氢能等很可能成为主要能源 |
| D.2011年11月3号1时43分神州八号与“天宫一号”完成了首次对接,神八在制造过程中使用了大量的复合材料 |
有关下列两个装置图的说法不正确的是()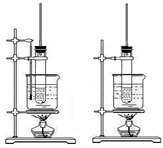
| A.左图可用于实验室制取硝基苯 |
| B.右图可用于实验室制取酚醛树脂 |
| C.长导管是起导气、冷凝回流作用 |
| D.制硝基苯和酚醛树脂均选择浓硫酸作催化剂 |
下列说法正确的是( )
A.淀粉、纤维素、蛋白质都是天然高分子化合物
B.煤经过气化、液化等物理变化可得到清洁燃料
C.石油分馏、石油裂化、石油裂解都是化学变化
D.棉花、羊毛、蚕丝、麻都由C、H、O元素构成
下图是六种常见有机化合物分子的球棍模型,下列有关叙述中不正确的是( )
| A.甲、乙、丙属于烃,丁、戊、己属于烃的衍生物 |
| B.丙和己混合后会分层,且丙在上层 |
| C.甲、丙、丁、戊、己均发生取代反应 |
| D.乙和水反应可生成丁,丁和戊反应可生成己 |