常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- |
| B.澄清透明的溶液:Cu2+、Mg2+、SO42-、Cl- |
| C.0.1 mol·L-1 Na2CO3溶液:NH4+、Fe2+、SO42-、NO3- |
| D.c(Fe2+)=1.0 mol·L-1溶液:H+、K+、Cl-、MnO4- |
在下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是
| A.硫在空气中燃烧 | B.铜片与浓硫酸共热 |
| C.红热的木炭与浓硫酸反应 | D.亚硫酸钠与稀硫酸反应 |
据报道,科学家已成功合成了少量N4,有关N4的说法正确的是
| A.N4是N2的同素异形体 | B.N4和N2是同种物质 |
| C.相同质量的N4和N2所含原子个数比为 1:2 | D.N4的摩尔质量是56 g |
下列块状金属中,在常温时能全部溶于足量浓HNO3的是
| A.Au(金) | B.Ag | C.Al | D.Fe |
标准状况下,1 mol SO2与1 mol SO3具有相同的
| A.体积 | B.质量 | C.分子数目 | D.原子数目 |
下列表示物质结构的化学用语或模型正确的是
| A.8个中子的碳原子的核素符号:12C | B.HF的电子式: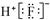 |
C.Cl-离子的结构示意图: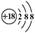 |
D.CH4分子的比例模型: |