下列陈述I、Ⅱ均正确且有因果关系的是
| 选项 |
陈述I |
陈述Ⅱ |
| A |
常温下铁与浓硫酸不反应 |
可用铁槽车密封运送浓硫酸 |
| B |
NaHCO3溶于水完全电离 |
NaHCO3是强电解质 |
| C |
NH4Cl为强酸弱碱盐 |
用加热法除去NaCl中的NH4Cl |
| D |
H2O2、SO2都能使酸性KMnO4溶液褪色 |
H2O2表现还原性,SO2表现漂白性 |
a g KNO3溶于b g水,形成V mL饱和溶液。下列关系式错误的是
A.KNO3物质的量浓度:c(KNO3)= mol·L-1 mol·L-1 |
B.20 ℃时KNO3的溶解度S=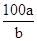 g g |
C.KNO3质量分数:w(KNO3)=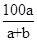 % % |
D.该溶液的密度ρ=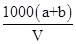 g·L-1 g·L-1 |
已知反应:2FeCl3+2KI===2FeCl2+I2+2KCl,H2S+I2===S+2HI,2FeCl2+Cl2===2FeCl3,由此得出下列微粒氧化性由强到弱的顺序为
| A.Cl2 > I2> Fe3+ > S | B.Cl2 > Fe3+ > I2 > S |
| C.Fe3+ > Cl2 > I2 > S | D.S > I2 > Fe3+ > Cl2 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向溶液X中先加盐酸酸化,无现象,再加入AgNO3溶液 |
白色沉淀 |
X中一定含Cl— |
| B |
向溶液Y中先加盐酸酸化,无现象,再加入BaCl2溶液 |
白色沉淀 |
Y中一定含SO42- |
| C |
溶液Z中加入碳酸钠溶液产生白色沉淀,再加盐酸 |
白色沉淀 消失 |
Z中一定含Ba2+ |
| D |
钠盐W溶液中,加入稀盐酸,并将产生的气体通入澄清石灰水 |
石灰水 变浑浊 |
W一定是Na2CO3 |
设NA表示的值,下列叙述正确的是
| A.标准状况下,2. 24LCH4含有的H原子数为0.1NA |
| B.常温常压下,NA个CO2分子占有的体积为22.4L |
| C.1 mol·L-1 A1Cl3溶液中含有的Cl-数目为3NA |
| D.2.4g金属镁变为镁离子时失去的电子数为0.2 NA |
下列中和反应的离子程式能以H++OH-===H2O表示的是
| A.醋酸和氢氧化钠溶液 | B.氢氧化镁和硝酸 |
| C.氢氧化钠溶液和稀硫酸 | D.氢氧化钡和稀硫酸 |