水与人类的生活和生产密切相关。2010年“中国水周”的宣传主题是“严格水资源管理,保障可持续发展”。为响应这一主题,某中学环保小组的同学配合环保部门,定期对流经我市的河水进行取样测试。请根据某日采集的水样回答以下问题:
(1)除去水样中难溶性的固体,需将水样(填序号)________;
①加热 ②过滤 ③蒸发 ④冷却
(2)在白瓷板上放一小片pH试纸,用玻璃棒蘸取少量(1)中所得到的液体,测得其pH大于7,则说明该水样显________性;
(3)由上述数据分析,该河水的主要污染物可能是(填序号)________;
①带有酸臭味的城市生活污水
②化工厂排放的污水
(4)为了保护河水水质,下列做法合理的是(填序号)________。
①抑制水中所有动、植物的生长
②不任意排放工业废水
③禁止使用农药和化肥
④生活污水经过净化处理后再排放
下面是几种实验室制取气体的发生装置和收集装置。请回答下列问题: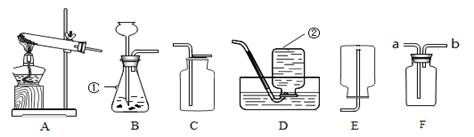
(1)指出图中标有数字②的仪器名称:。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气时的发生装置应选用(填字母标号),该反应的化学方程式;若用装满水的F装置收集氧气,则水会从(填“a”或“b”)端被排出。
(7分)某实验小组利用图1所示仪器配制一定溶质质量分数的氯化钠溶液。
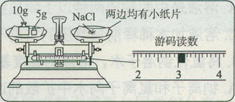
图 1图2
(1)图1中缺少一种必须用到的玻璃仪器,它是
(2)图2中的操作错误是;若按图2操作,取用的氯化钠实际质量为g。
(3)量取蒸馏水的体积读数如图3所示,则该实验小组原计划配制的氯化钠溶液的溶质质量分数为(水的密度为1 g/cm3),而实际得到溶液的溶质质量分数为
图3
(4)在上述实际配得的溶液中加6.0g水,则溶液的溶质质量分数为
(5)在上述实际配得的溶液中加23.0g氯化钠,则溶液的溶质质量分数为
(已知:25℃时,氯化钠的溶解度是36g。计算结果均保留一位小数)
(9分)纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。
请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2+_________+CO2=CaCO3↓+__________+H2O
(2)若在实验室中进行该实验,操作l的名称是___________,使用到的非玻璃实验用品有_________、________。
(3)上述过程制得的碳酸钙粗品表面可能含有的可溶性杂质有___________(写一种化学式即可)。操作2为:_________、检验和干燥,检验操作中选用的试剂为____________(选择序号)。①NH4Cl溶液 ②AgNO3溶液 ③CaCl2溶液④Ba(NO3)溶液
(4)上述流程中的副产品可用作__________________________________。(写一种用途)
(6分)现有六种物质,选择相应物质的字母填空
| A.活性炭 | B.高锰酸钾 | C.石油 | D.聚乙烯塑料 E.干冰 F.酒精 |
(1) 可用于人工降雨(2) 是实验室最常用的燃料
(3) 被誉为“工业的血液”(4) 可用于吸附冰箱内的异味
(5) 可用于实验室制取氧气(6) 可用作食品包装袋
某市一家大型化工厂处理回收含铜废料的生产流程如下:
过程(1)得到的残留物不溶于水和稀硫酸;过程(2)是黑色固体与稀硫酸加热生成硫酸铜和水。请写出上述生产流程中与铜直接有关的化学方程式。
(1)
(2)
(3)