下面是实验室制取和收集气体的装置,根据所学知识回答下列问题:
(1)写出仪器的名称:a ;b
(2)从上图中选择装置制取并收集干燥的CO2,应选用图中的 (填字母)。
(3)实验室若用装置E收集H2,气体应从导管的 (填“d”或“e”)端进入。
(4)若制取的O2用B装置制取的反应原理 ,用F装置排水法收集,请将图F补画完整(直接在图中画出)。
(5)化学兴趣小组为了测定石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应)。随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图所示。请完成下列计算内容:(写出计算过程)
①样品中碳酸钙的质量分数是多少?
②所用稀盐酸溶质的质量分数是多少?
下图所示的实验中,反应前氧化铁和碳粉的质量分别为32克和1.2克,反应后得到气体A和28.8克黑色固体B。
(1)白色沉淀的质量为g;
(2)推断黑色固体B的化学式。(要求写出推断过程)
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数。
(1)配制200g质量分数为8%的氢氧化钠溶液。
①计算:需要氢氧化钠固体的质量为g,水的体积为mL(水的密度近似看作1g/cm3)。
②称量:调节托盘天平平衡,然后(按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是.
③溶解:用量筒量取所需的水,倒入盛有氢氧化钠固体的烧杯里,搅拌,使其溶解,并冷却至室温。
④把配好的溶液装入试剂瓶,塞好橡皮塞并贴上标签。
(2)如图表示用上述配制的氢氧化钠溶液与20 g某稀盐酸发生反应后溶液温度的变化情况。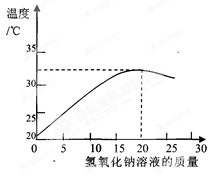
①根据曲线判断,当加入氢氧化钠溶液的质量为时,反应恰好完全进行。
②当加入15 g氢氧化钠溶液时,所得溶液中的溶质为(写化学式)。
③试计算上述完全反应后所得溶液的溶质质量分数(请写出计算过程)。
为检查某石灰石样品中碳酸钙的纯度,取该样品24g放入烧杯中,再向烧杯中加入70g稀盐酸,恰好完全反应(杂质不参加反应),反应后烧杯中剩余固体物质共85.2g,
(1)反应生成CO2的质量为g;
(2)石灰石样品中碳酸钙的质量。
(3)石灰石样品中碳酸钙的质量分数
鸡蛋壳的主要成分是碳酸钙,为了测定鸡蛋壳中碳酸钙的含量,小丽称取30g干燥的碎鸡蛋壳放入烧杯中,并向其中加入了80g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量为101.2g。我能完成下列计算:
⑴碳酸钙的质量;
⑵当碳酸钙恰好完全反应时所得溶液中溶质的质量分数。(结果保留一位小数)
甲醛是室内装修的隐形杀手,甲醛的化学式为CH2O。
⑴甲醛中碳、氢、氧的质量比为;
⑵甲醛中碳元素的质量分数为。