鸡蛋壳的主要成分是碳酸钙,为了测定鸡蛋壳中碳酸钙的含量,小丽称取30g干燥的碎鸡蛋壳放入烧杯中,并向其中加入了80g稀盐酸恰好完全反应(假设鸡蛋壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应),反应后烧杯中物质的总质量为101.2g。我能完成下列计算:
⑴碳酸钙的质量;
⑵当碳酸钙恰好完全反应时所得溶液中溶质的质量分数。(结果保留一位小数)
如图是一瓶医用注射盐水标签的部分内容。完成下列填空:
(1)氯化钠中钠、氯元素的质量比是;
(2)该瓶盐水能给病人提供钠元素的质量是g (精确到0.1g)
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验,反应的化学方程式是2H2O2 O2↑+2H2O.请计算:
O2↑+2H2O.请计算: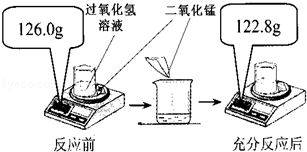
(1)反应后产生氧气的质量为g。
(2)此过氧化氢溶液的溶质质量分数。
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应制备:Al2O3+N2+3C 2AlN+3CO,若要得到41Kg的氮化铝,则至少需要参加反应的氧化铝(Al2O3)的质量为多少千克?
2AlN+3CO,若要得到41Kg的氮化铝,则至少需要参加反应的氧化铝(Al2O3)的质量为多少千克?
工业上可用二氧化硫生产硫酸,反应的化学方程式为:2SO2+O2+2H2O=2H2SO4。欲将16吨二氧化硫气体完全转化为硫酸,则参加反应的氧气的质量是多少?
某兴趣小组对硫酸厂排放的废水中硫酸含量进行检测:
(1)配制溶液:配制溶质质量分数为4%的NaOH溶液20g,需要NaOH固体g,水ml(水的密度为1g/cm3);
(2)检测分析:取废水样品98g,恰好与配制的20gNaOH溶液完全反应,试计算废水中硫酸的质量分数。(假设废水中其它成分均不和NaOH反应,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O).