为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂。对实验现象的“解释或结论”错误的是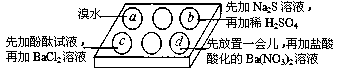
| |
实验现象 |
解释或结论 |
| A |
a中溴水褪色 |
还原性:SO32—> Br— |
| B |
b中加硫酸后产生淡黄色沉淀 |
SO32—和S2—在酸性条件下发生反应 |
| C |
c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 |
SO32—+H2O HSO3—+OH—,所以滴入酚酞变红; HSO3—+OH—,所以滴入酚酞变红;Ba2++SO32— = BaSO3↓,水解平衡向左移动,红色褪去 |
| D |
d中产生白色沉淀 |
Na2SO3溶液已被氧化变质 |
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6 mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.上述电解过程中共转移2 mol电子 |
| B.原混合溶液中c(K+)为2 mol/L |
| C.电解得到的Cu的物质的量为0.5 mol |
| D.电解后溶液中c(H+)为2 mol/L |
已知:Fe2O3(s)+ 3/2C(s)= 3/2CO2(g)+2Fe(s) △H=" +234.1" kJ/mol
C(s)+O2(g)=CO2(g) △H=" -393.5" kJ/mol
则反应2Fe(s)+ 3/2O2(g)=Fe2O3(s)的△H是
| A.-169.4 kJ/mol | B.-627.6 kJ/mol |
| C.-744.7 kJ/mo | D.-824.4 kJ/mol |
已知某酸H2B在水溶液中存在下列关系:①H2B H++HB-,②HB-
H++HB-,②HB- H++B2-。关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是
H++B2-。关于该酸对应的酸式盐NaHB的溶液,下列说法中一定正确的是
A.NaHB属于弱电解质
B.溶液中的离子浓度c(Na+)>c(HB-)>c(H+)>c(OH-)
C.NaHB和NaOH溶液反应的离子方程式为H++OH-===H2O
D.c(Na+)=c(HB-)+c(B2-)+c(H2B)
在容积一定的密闭容器中,反应2A 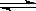 B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
B(g)+C(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述正确的是
| A.正反应是吸热反应,且A是气态 |
| B.正反应是放热反应,且A不是气态 |
| C.其他条件不变,加入少量A,该平衡不移动 |
| D.改变压强对该平衡的移动无影响 |
pH相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是
| A.反应结束后溶液的pH:甲>乙 | B.反应开始时的速率:甲>乙 |
| C.反应所需时间:甲<乙 | D.反应开始时,酸的物质的量浓度:甲>乙 |