蒽( )反应生成化合物X(立体对称图形),如下图所示:
)反应生成化合物X(立体对称图形),如下图所示: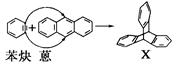
(1)蒽与X都属于________(填选项,下同)。
A.环烃 B.烷烃 C.芳香烃
(2)苯炔的分子式为________,苯炔不具有的性质是________。
A.能溶于水 B.能发生氧化反应
C.能发生加成反应 D.常温常压下为气体
(3)1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列 事实。
A.苯不能使溴水褪色 B.苯能与H2发生加成反应
C.溴苯没有同分异构体 D.邻二溴苯只有一种
现代化学认为苯分子碳碳之间的键是 。
(4)下列属于苯的同系物的是________。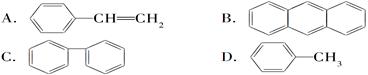
(5)能发生加成反应,也能发生取代反应,同时能使溴水因反应而褪色,也能使酸性高锰酸钾溶液褪色的是________。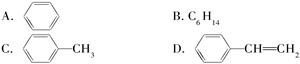
它是生产某塑料的单体,写出合成该塑料的化学方程式:__________________________。
国家游泳池水质标准:
| 游离性余氯 |
0.3~0.5 mg·L-1 |
| pH |
6.5~8.5 |
| 浑浊度 |
≤5度 |
| 细菌总数 |
≤1 000个/mL |
| 大肠菌群 |
≤18个/mL |
| 硫酸铜剂量 |
0.25~0.50 mg·L-1,最大加药量不超过1.0 mg·L-1 |
*游离性余氯:包括ClO-及HClO等。
请参考表中有关信息回答以下问题:
(1)游泳池一般用漂白精作为消毒剂,漂白精的有效成分是Ca(ClO)2,其消毒原理是_________________________________。
(2)池中加入硫酸铜的目的是__________________,如果加入硫酸铜的剂量过大会对人体产生有害作用,其原因是什么?_________________________________。
(3)某游泳池注满水,水的总体积为1.50×103 m3,该游泳池消毒一次所用的漂白精,理论上需用多少升标准状况下的氯气和多少克氢氧化钙来制取?(列式计算)(池水的密度为1.00 g·cm-3,游离性余氯按ClO- 0.50 mg·L-1计)
某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:_____________。B内只需加入一种固体试剂,该试剂的名称为__________,B中能产生氨气和氧气混合气体的原因(结合化学方程式回答)___。
②按气流方向连接各仪器(填接口字母)
(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下: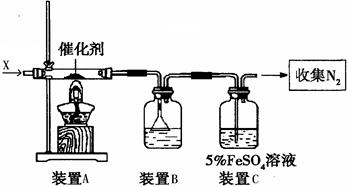
①装置C的作用可能是 ____________
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据
4NO2(g);△H>0,下表为反应在某温度下的部分实验数据
| t/s |
0 |
500 |
1000 |
| c(N2O3)/mol·L-1 |
5.00 |
3.52 |
2.48 |
计算在t=500s时,NO2的反应速率为
在工业上烯烃可以合成多种有机材料。
(1)某同学设计了由乙烯合成Y的3条路线(I、II、III)如下图所示。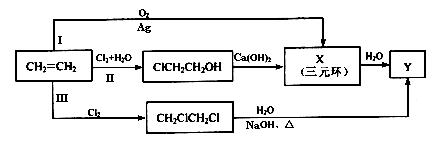
① 3条合成路线中,你认为符合“原子经济”
要求的合成路线是(填序号“I”、“II”或“III”)。
② X的结构简式是。
(2)已知Q为乙烯的同系物,以Q和X为原料合成M的方法如下: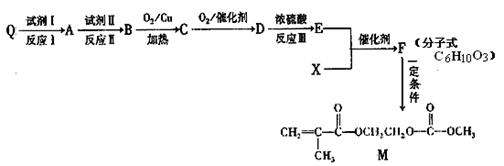
请回答下列问题:
①Q的名称是
②E中含有官能团的名称是,F的结构简式是 .
③写出M与足量氢氧化钠溶液反应的化学方程式
④已知:
G的同分异构体有多种,写出符合下列条件的G的所有同分异构体
a.与钠反应放出氢气 b.在酸性条件下水解为N和乙醇c. N中含有支链
金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航海、化工、医疗上不可缺少的材料。
I、工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:
其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:_________(填“需要”或“不需要”)
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的离子方程式。
II、为了提高资源的利用率,减少环境污染,可将氯碱厂、炼钛厂和甲醇厂组成产业链,其关系如下图所示。
(3)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________________________。
(4)已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=一641 kJ·mol-1
②1/2Ti(s)+Cl2(g)=1/2TiCl4(l);△H=一385 kJ·mol-1
则Mg 与TiCl4反应的热化学方程式为,
该反应在氩气氛中进行的理由是。
(5)在上述产业链中,合成192 t 甲醇理论上需额外补充H2t (不考虑生产过程中物质的任何损失)。
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是445.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s) + H2SO4(98%)==Na2SO4 + H2O + SO2↑
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是_______________、_______________、_______________。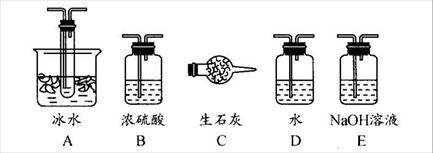
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是。
(3)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
(5)尾端球形干燥管的作用是。