关于离子键、共价键的各种叙述中,下列说法中正确的是
| A.在离子化合物里,只存在离子键,没有共价键 |
| B.非极性键只存在于双原子的单质分子(如Cl2)中 |
| C.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
| D.由不同元素组成的含多个原子的分子里,一定只存在极性键 |
实验测得气态无水氯化铝在1.01×105Pa、不同温度(t3>t2>t1)时的密度(ρ)和气体摩尔体积(Vm)数据见下表。
| t/℃ |
t1 |
t2 |
t3 |
| ρ/ |
5.00 |
2.67 |
1.48 |
| Vm/ |
53.4 |
70.0 |
90.0 |
可见,t2℃时无水氯化铝存在形式的化学式为()
| A.AlCl3 | B.AlCl3和Al2Cl6 | C.Al3Cl9 | D.Al2Cl6 |
下列条件下,两种气体的分子数一定不相等的是
| A.相同质量、不同密度的N2O和CO2 |
| B.相同体积、相同密度的CO和C2H4 |
| C.相同温度、相同压强、相同体积的O2和O3 |
| D.相同压强、相同体积、相同质量的NO2和N2O4 |
如下图所示,6个编号分别代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应(已知高温下氨气能还原氧化铁)。a.Alb.Fe2O3c.NaOH溶液d.氢碘酸溶液e.NH3f.Cl2,图中⑤表示的物质是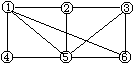
| A.a或b | B.c | C.d | D.e或f |
下列有关分散系中几个基本概念的分析,其中正确的是
| A.若A中混有少量的B,可采用冷却热饱和溶液法提纯A 温度 20℃ 50℃ A的溶解度 35.7g 46.4g B的溶解度 31.6g 108g |
B.上述两种盐在相同温度下配制的饱和溶液的浓度不可能相同 |
| C.氯化钠溶液、水等分散系不能发生丁达尔现象 | |
| D.在Fe(OH)3胶体中滴加入少量H2SO4将有沉淀产生 |
用NA表示阿伏加德罗常数,以下各说法中正确的是
| A.常温常压下,11.2 L氯气含有的分子数目大于0.5NA |
| B.常温常压下,2.24 L四氯化碳中所含氯原子数大于0.4 NA |
| C.0.1mol的铜与足量的浓硫酸反应生成SO2的体积约为22.4L |
| D.在同温同压下,相同体积的任何气体单质应含有相同的原子数 |