实验室使用块状石灰石(CaCO3)和稀盐酸制CO2,当观察不到有气泡产生,固体仍有剩余时,通常认为反应结束,剩余液呈中性。某兴趣小组对此进行了以下探究:
【实验操作】(1)向试管中加入5粒石灰石,倾倒约试管体积1/3的稀盐酸(1:1);观察不到气泡后,仍有固体剩余;将试管静置。
(2)取上层清液,用pH试纸测得溶液pH=2,说明溶液显_______性;
pH测定中,“上层清液滴到试纸上”的后一步操作是_______________。
【实验思考Ⅰ】反应剩余液中有哪些物质?其中能使溶液pH=2的有哪些?
【实验探究Ⅰ】(1)甲同学通过实验排除了CaCl2的可能性。简述其实验方案___________。
(2)乙同学将CO2通入蒸馏水中至饱和,测得pH>5,。
(3)综合甲、乙两同学实验,得出的结论是:剩余液中还含有_______________。
【实验思考Ⅱ】试管中剩余固体是否仍含有CaCO3?
【实验探究Ⅱ】小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生。
(1)由此得出的结论是______________;写出反应的化学方程式_______________________。
(2)比较稀盐酸加入前后的实验现象,解释“又有大量气泡产生”的原因:_________________。
【拓展延伸】(1)反应剩余液放置一段时间后,溶液pH增大,其主要原因是_________。
(2)假如用100g14.6%的稀盐酸和足量的石灰石反应,看不到气泡产生时,停止收集气体。收集到的CO2质量_______(选填“>”、“<”、“=”)8.8g。
根据如图装置,结合所学化学知识回答问题。

(1)写出仪器①的名称 ;
(2)实验室制取氧气的方法有多种方法,从“低碳”角度分析,最佳方法是(用化学方程式表示): ;若用装置C收集氧气,验满的方法为: ;
(3)在实验室可以用加热固体无水醋酸钠和固体碱石灰的方法制取甲烷。通常情况下,甲烷的密度比空气小,难溶于水,实验室制取甲烷选择的发生装置是 (填字母);若用F装置收集甲烷,气体应从 口进入(填“a”或“b”)。
增氧剂可用于给鱼池增氧,某化学兴趣小组对某种增氧剂的增氧原理进行实验探究。
【查阅资料】该增氧剂的主要成分是过碳酸钠,过碳酸钠是一种白色晶体,化学式可以表示为2Na 2CO 3•3H 2O 2。过氧化氢溶液常温较稳定,能缓慢分解,受热容易分解。
【提出问题】增氧剂真的能增氧吗?
【初次探究】取少量增氧剂于试管中,加入足量蒸馏水,观察到固体完全溶解,形成无色溶液,无气泡产生;加热,产生大量气泡。
【作出猜想】该兴趣小组结合资料和实验现象推测增氧剂溶于水后生成Na 2CO 3和H 2O 2。
【再次探究】该兴趣小组进行如表实验:
|
实验操作 |
实验现象 |
实验结论 |
|
|
(1) |
另取少量增氧剂于试管中,加入足量蒸馏水,待其完全溶解,再加入 ,将带火星的木条伸入试管内 |
|
溶液中含有H 2O 2。该操作中H 2O 2参与反应的化学方程式为 |
|
(2) |
待步骤(1)完全反应后,将所得物质过滤,取少量滤液于另一支试管中,加入 |
产生白色沉淀 |
溶液中含有Na 2CO 3 |
【得出结论】该增氧剂的增氧原理为 。
【评价反思】该增氧剂的保存方法为 。
实验室现有氯酸钾、二氧化锰、稀硫酸、石灰石、稀盐酸、锌粒以及如图仪器及装置,据图回答问题:

(1)利用上述仪器和药品制取CO2,选择的仪器是 (填序号)。
(2)利用上述仪器和药品制取O2,还缺少一种仪器,其名称为 。该反应的化学方程式为 。
(3)如果用装置⑨采用排空气法收集H2,则H2从导管口 进入(填“a”或“b”)。
以黄铜矿(主要成分为CuFeS2)为原料,采用生物炼铜是现代炼铜的新工艺,同时还可以获得绿矾(FeSO4•7H2O),流程如图:

(1)步骤①中的化学方程式:4CuFeS2+17O2+2H2SO4 4CuSO4+2Fe2(SO4)3+ 。
4CuSO4+2Fe2(SO4)3+ 。
(2)步骤②中的反应有两个:反应一是Fe+Fe2(SO4)3═3FeSO4,该反应属于 (填基本反应类型),反应二的化学方程式为 。
(3)加入的A是 (填化学式)。
(4)获得绿矾的“一系列操作”为:蒸发浓缩、 、过滤等。
某班同学在做“某些酸、碱、盐之间是否发生反应”的探究实验时发现,酸碱之间的反应,往往没有明显的现象。那么如何判断酸碱发生了化学反应呢?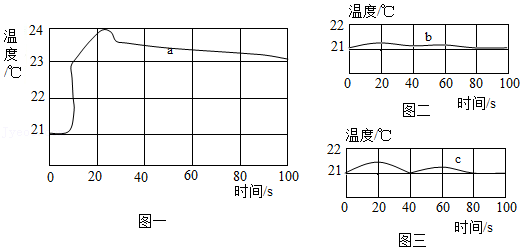
【提出问题】如何判断酸、碱溶液发生了化学反应?
【实验药品】一定质量分数的稀盐酸、一定质量分数的氢氧化钠溶液(稀)、酚酞溶液、蒸馏水。
【实验探究】
(1)甲小组在烧杯中加入50mL氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入稀盐酸,发现 (填现象),证明氢氧化钠溶液与稀盐酸发生了化学反应,该反应的化学方程式为 。
(2)乙小组进行了以下三个实验,并用温度传感器测定实验过程中的温度变化情况,得到了如图所示的三条曲线。
实验一:50mL稀盐酸与50mL氢氧化钠溶液混合(曲线a);
实验二:50mL稀盐酸与50mL蒸馏水混合(曲线b);
实验三:50mL氢氧化钠溶液与50mL蒸馏水混合(曲线c)。
结合实验目的分析,增加实验二、实验三的目的是 。
对比三条曲线,可以得到如下结论:
①氢氧化钠溶液和稀盐酸一定发生了化学反应。
②酸碱中和反应是 反应(填“放热”或“吸热”)。
【交流与反思】
(3)甲小组认为,通过实验探究(2)得出“中和反应是放热反应”的结论不严谨,应该补充 实验。