化学课外小组设计了一套如图所示的气体发生及收集装置,并探究该装置的多功能性.
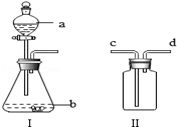
(1)甲同学认为装置Ⅰ可作为实验室制取O2的发生装置,则Ⅰ的a仪器中应加入 ,b仪器中应加入 ,反应的化学方程式为 ,装置Ⅱ中从 管口进气即可作为O2的收集装置.
(2)乙同学认为装置Ⅰ可作为实验室制取二氧化碳的发生装置,则Ⅰ的a仪器应加入 ,b仪器中应加入 .
(3)如果要用装置Ⅱ收集H2,则应从 管口进气.
某实验小组根据下图所示装置探究燃烧的条件,请回答问题。
(1)检查装置气密性后,燃烧匙中放入少量的白磷,小烧杯内放入适量的碳酸钠粉末,组装好装置。打开弹簧夹,将溶液A缓慢加入到小烧杯内,溶液A是______,一段时间后,______(填写后续实验步骤和现象),关闭分液漏斗的活塞、弹簧夹,然后用凸透镜加热白磷,观察到白磷不燃烧,该实验过程的目的是______。
(2)停止加热,轻轻振荡装置,一段时间后打开弹簧夹,再用凸透镜加热白磷,观察到白磷燃烧,白磷燃烧的原因是______,该实验过程中发生反应的化学方程式为______。
实验室模拟炼铁原理进行实验,得到的尾气是CO、CO2的混合气体。现利用下图所示装置将混合气体进行分离,并得到干燥的气体。
(1)检查装置的气密性。A、B、C装置内放入一定量水,使长导管浸没在水面以下,关闭k2、k4,打开k1、k3,并在最右端导管口接注射器。当向外缓慢拉动注射器活塞时,若观察到 ,则说明整套装置气密性良好。
(2)装入药品。C中所盛试剂X为 。
(3)分离两种气体。请完成下表(实验操作只需答出关闭和打开活塞即可)。
| 实验操作 |
分离出的气体 |
(4)在实验过程中,A中发生反应的化学方程式为 。
某小组同学利用如图所示装置探究铁生锈的条件,其中C、D的分液漏斗中为足量且浓度和体积均相同的稀盐酸。
(1)步骤一:关闭K2和K3,打开K1,A中反应的化学方程式是 ,B中所盛放的试剂是 。对比铁丝表面的变化,能够说明铁生锈与水有关的是装置 和 (填C、D或E,下同),能够说明铁生锈的快慢与氧气浓度有关的是装置 和 。
(2)步骤二:关闭K1,打开K2和K3,将装置C、D中分液漏斗内的稀盐酸同时全部注入广口瓶中,两个广口瓶中现象的不同点是:① ;② ,由此也可以判断铁丝生锈情况。C中反应的化学方程式是 。
(3)温度会影响铁生锈的快慢,请设计实验加以证明: 。
某化学兴趣小组同学利用如下图所示装置进行实验。
(1)打开a,关闭b,装置I中加入黑色固体和无色液体,装置Ⅱ的热水中加入白磷,观察到Ⅱ中白磷燃烧。
①装置I中发生反应的化学方程式为 。
②白磷燃烧的原因是 。
(2)装置I中加入大理石和过量稀盐酸,装置Ⅱ 中加入滴有无色酚酞的氢氧化钠溶液。
①打开a,关闭b,Ⅱ中发生反应的化学方程式为 。
②一段时间后,关闭a,打开b。若装置Ⅱ中最终得到无色澄清溶液,则Ⅱ中一定发生的反应化学方程式为 ;若装置Ⅱ中最终得到无色溶液且底部有不溶物,则II中无色溶液的溶质可能为 。
某化学兴趣小组的同学对呼吸面具的制氧原理产生好奇心,通过查阅资料得知,呼吸面具中制取氧气的主要原料是固体过氧化钠(Na2O2)。过氧化钠分别能和二氧化碳、水反应都生成氧气,反应的化学方程式为:
2Na2O2+2H2O 4NaOH+O2↑ 2Na2O2+2CO2
4NaOH+O2↑ 2Na2O2+2CO2 2Na2CO3+O2
2Na2CO3+O2
为了测定呼吸面具中过氧化钠的质量分数,该小组的同学在老师的指导下,利用下图所示装置(固定装置一略去)开展探究,并得到正确的结论。
已知,装置B中盛有饱和NaHCO3溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO组成的混合物。整套装置气密性良好,反应所需试剂均足量。
请回答下列问题:
(1)仪器a的名称是 ,装置A的作用是 ;
(2)不用装置E代替装置C的理由是 。
(3)装置D中过氧化钠药品的质量为mg,装置D在反应前后的总质量n1g和n2g。若药品中所含杂质既不溶于水也不参加化学反应,则药品中过氧化钠的质量分数= 。