常温下,Ksp(CaSO4)=9×l0-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图。下列判断错误的是
| A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 |
| B.a点对应的Ksp等于c点对应的Ksp |
| C.向d点溶液中加入适量CaCl2固体可以变到c点 |
| D.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×l0-3mol/L |
2015年诺贝尔生理学或医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素。以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如右图)。下列说法正确的是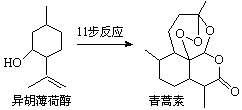
| A.异胡薄荷醇的分子式为C10H17O |
| B.异胡薄荷醇在NaOH醇溶液中可发生消去反应 |
| C.青蒿素分子中含有7个手性碳原子 |
| D.青蒿素在热的酸、碱溶液中均可稳定存在 |
下列有关氯气及其含氯分散系的说法正确的是
| A.钢铁在Cl2气氛中主要发生电化腐蚀 |
| B.在新制氯水中加入少量CaCO3,溶液中c(HClO)增大 |
| C.反应3Cl2(g) + 8NH3(g) = 6NH4Cl(s) + N2(g)的△H>0,△S<0 |
D.0.1mol·L-1NaClO溶液中:c(HClO) + c(H+) = c(OH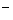 ) ) |
H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) △H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法正确的是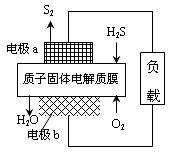
| A.电极a为电池的正极 |
B.电极b上发生的电极反应为:O2+2H2O+4e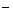 =" 4" OH =" 4" OH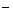 |
| C.电路中每流过4mol电子,电池内部释放632kJ热能 |
| D.每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
下列指定反应的离子方程式正确的是
A.MnO2与浓盐酸混合加热:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| B.(NH4)2Fe(SO4)2溶液中加入过量的NaOH溶液:Fe2++2OH-=Fe(OH)2↓ |
| C.Ba(HCO3)2溶液中加入稀硫酸:Ba2+ + SO42-= BaSO4↓ |
| D.H2C2O4(弱酸)溶液中加入酸性KMnO4溶液:2MnO4-+ 5H2C2O4= 2Mn2+ + 10CO2↑+ 2H2O + 6OH- |
利用海洋资源获得的部分物质如下图所示,有关说法正确的是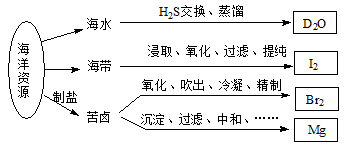
A.在化学反应中, H2O可转变为D2O H2O可转变为D2O |
| B.“加碘食盐”生产中碘添加剂为单质I2 |
| C.实验室用带玻璃塞的棕色瓶贮存液Br2 |
| D.电解饱和MgCl2溶液时在阴极得到Mg |