某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
(1)小明同学用图中的发生、收集装置。甲、乙两试管各有两根导管,连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体。则稀硫酸应置于 中(填“甲”或“乙”);G管可以用化学实验室里的一种常用仪器代替,你认为这种仪器的名称是 。仪器甲、乙接口的连接方式如下:A连接 ,C连接F;(填写接口的编号)
(2)小李同学用沉淀法测定Na2SO3的质量分数。
操作流程:
①操作Ⅱ的名称是 。
②操作Ⅰ之前,为判断所加BaCl2溶液是否过量, 设计如下方案,其中最合理的是 。
A.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
B.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
③根据以上数据得出Na2SO3的质量分数为 。
④小丽同学经认真分析,上述实验操作均正确,但发现实验结果与预期相差较大,请你推测可能的原因是 ,验证方法 。
我国化学侯德榜(右图)改革国外的纯碱生产工艺,生产流程可简要表示如下: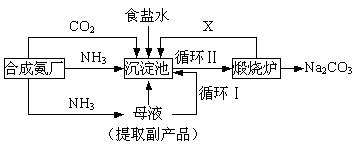

沉淀池中四种盐在不同温度下的溶解度(g / 100 g水)表
 |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
100℃ |
| NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
39.8 |
| NH4HCO3 |
11.9 |
15.8 |
21.0 |
27.0 |
-① |
- |
- |
- |
| NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
16.4 |
- |
| NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.3 |
77.3 |
①>35℃NH4HCO3会有分解
请回答:
(1)沉淀池中反应温度控制在30℃~35℃,是因为若高于35℃,则,若低于30℃,则;为控制此温度范围,采取的加热方法为。
(2) 沉淀池中发生的化学反应方程式是。
(3)副产品的一种用途为,写出上述流程中X物质的分子式。
(4)加料完毕后,继续保温30分钟,目的是。静置后只析出NaHCO3晶体的原因是。用蒸馏水洗涤NaHCO3晶体的目的是除去杂质(以化学式表示)。
(5) 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加。
如图所示,将甲、乙两 个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定,溶液浓度相同)。
个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定,溶液浓度相同)。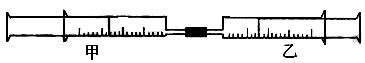
试回答下列问题:
| 实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
| 1 |
10mLFeSO4溶液 |
10mLNH3 |
生成白色沉淀,后变色 |
| 2 |
10mLAlCl3溶液 |
40mLNaOH溶液 |
|
| 3 |
10mL紫色石蕊试液 |
25mLCl2 |
|
| 4 |
15molCl2 |
40mLNH3 |
⑴实验1中,沉淀最终变为色,写出沉淀变色的化学方程式。
⑵实验2甲针筒内的现象是:,写出有关反应的离子方程式:、。
⑶实验3甲针筒内的现象是:,反应后乙针筒内有少量的残留气体,正确的处理方法是将其通入溶液中 。
。
⑷实验4中,已知:3Cl2+2NH3=N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为。
某次实验需用0.4 mo l·L-1 NaOH溶液480 mL。配制方法如下:
l·L-1 NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_______________mL容量瓶;
(2)用托盘天平准确称量__________g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待__________________后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯次,洗涤后的溶液___________________,轻轻晃动容量瓶,使 溶液混合均匀;
溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面________________________时,改用___________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,______________________________;
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是___________,偏低的是___________,对实验结果没有影响的是___________(填各选项的序号)。
| A.所用的NaOH中混有少量Na2O |
| B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥 |
| C.配制溶液所用的容量瓶洗净后没有烘干 |
| D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作 |
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
选择下列实验方法分离物质,将分离方法的字母代号填在横线上。
| A.结晶 | B.过滤 | C.蒸馏 | D.分液 |
(1)分离饱和食盐水和沙子_______________。
(2)分离水和汽油______________。
(3)分离CCl4(沸点76.75℃)和甲苯(沸点110.6℃)____________。
(4)从硝酸钾和氯化钠的混合溶液中获得硝酸钾______________。
一定量的浓硫酸与足量Zn充分反应时,有SO2和H2生成。
某校化学研究性学习小组对此进行研究。
按图组装好实验装置,微热试管A,观察到C、D、E中均有气泡产生;随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失;反应较长时间后,C、D、E中的气泡量又会明显增加。
试回答:
(1)从甲、乙中选择合适的装置填入B、C中,并进行正确连接,a接、接b,c接、接d;D、E两支试管中CCl4溶液的作用是
。
(2)能证明浓硫酸具有强氧化性的实验现象为反应较长时间后气泡量又会明显增加的原因是
(3)D中浑浊消失的离子方程式 为
为