(18分)自然界中化合态硫主要以FeS2(黄铁矿)、CuFeS2(黄铜矿)等矿物形式存在。用黄铜矿炼铜的总反应为: 。
。
(1)该反应中_______元素被还原,如果在反应中生成1molCu,转移电子数为____(用NA表示阿伏加德罗常数)。
(2)上述产生的SO2是一种大气污染物,不能直接排放到大气中,目前工业上常用的处理方法有多种。
I、用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4
①写出上述转化中生成NH4HSO3的化学方程式_______(用一个方程式表示)若想提高该过程中SO2的除去速率,可采取的措施为_______(填序号)
| A.增大氨水浓度 |
| B.升高反应温度 |
| C.使气体与氨水充分接触 |
| D.通入空气使HSO3-转化为SO42- |
②25℃时0.lmol·L—1 (NH4)2SO4溶液的pH=5,其原因是_______(用离子方程式表示),若水解常数用Kb表示,则该溶液中铵根离子的水解常数Kb约为______________.
Ⅱ、“钠碱法”:用NaOH溶液作吸收剂吸收SO2
③当n(NaOH):n(SO2)=_______时,吸收SO2的成本最低,所得吸收液中各离子浓度大小关系是_______,向吸收液中加入NaOH可得到_______。
下列物质不能由单质直接化合生成的是①SO2②SO3③CS2④Fe2S3⑤CuS⑥Al2S3
| A.①③⑤ | B.③④ | C.②④⑤ | D.①②⑤⑥ |
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P-P 198kJ·mol—1、P-O 360kJ·mol—1、氧气分子内氧原子间的键能为498kJ·mol—1。则P4(s)+ 3O2(g) ="=" P4O6(s)的反应热∆H为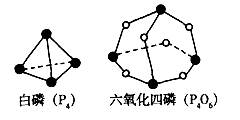
| A.+1638 kJ·mol-1 | B.-1638 kJ·mol-1 |
| C.-126 kJ·mol-1 | D.+126 kJ·mol-1 |
2006年9月份,“SK—Ⅱ”化妆品事件一时闹得沸沸扬扬。其实,从毒韭菜到炸鸡翅、从儿童奶粉到“瘦肉精”事件,化学性污染事件报道层出不穷,其中尤以食品安全最为引人恐慌。如食品报道中不断有①“致癌农药”、②“苏丹红”、③“碘元素”、④“亚硝酸盐”等化学名词出现。上述化学名词所提到的物质中,在某食品添加剂中允许含有但符合限量时不会引起中毒的是
| A.②③④ | B.②③ | C.③④ | D.只有③ |
实验室可以使用如右图所示装置制取的气体,且药品选用也正确的是k*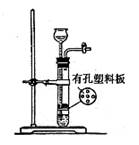
| A.O2:二氧化锰和双氧水 | B.SO2:亚硫酸钠和稀硫酸 |
| C.CO2:大理石和稀硫酸 | D.H2S:硫化亚铁和稀硫酸 |
设NA为阿伏加德罗常数,下列说法一定正确的是
| A.在1mol/L的FeCl3溶液中,Fe3+的个数小于NA |
| B.1 mol单质铜与足量硫或氯气反应失去电子数均为2NA |
| C.1mol碳烯(:CH2)中含有电子数为8NA |
| D.在标准状况下,22.4 L NO与11.2 L O2充分反应后,所得气体的分子数为NA |