已知:CO(g)+H2O(g) CO2(g)+H2(g) ∆H=– 41 kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) ∆H=– 41 kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡过程体系能量的变化 |
|||
| n(CO) |
n(H2O) |
n(CO2) |
n(H2) |
||
| ① |
1 |
4 |
0 |
0 |
放出热量:32.8 kJ |
| ② |
0 |
0 |
1 |
4 |
热量变化:Q1 |
| ③ |
1 |
1 |
2 |
1 |
热量变化:Q2 |
下列说法中,不正确的是
A.若容器①中反应10min达到平衡,0至10min时间内,用CO表示的平均反应速率υ(CO)=4.0×10-2 mol/(L·min)
B.容器③中,开始时υ(CO)生成>υ(CO)消耗
C.达平衡过程体系能量的变化:Q1=4Q2
D.平衡时,①与②容器中CO的体积分数相等
下列事实或过程与盐类水解无关的是
| A.热的纯碱溶液的洗涤油污能力更强 |
| B.误将钡盐(BaCl2)后,常用0.5% Na2SO4溶液解毒 |
| C.铵态氮肥不能和草木灰混合施用,否则会降低肥效 |
| D.配制FeCl3溶液时,通常需要加一些盐酸 |
 在一定温度下,HCN
在一定温度下,HCN 在水中存在电离平衡:HCN
在水中存在电离平衡:HCN H+ + CN-。下列说法错误的是
H+ + CN-。下列说法错误的是
A.通入HCl气体,Q>K,平衡逆向移动 |
B.升高温度,溶液pH减小 |
C.稀释溶液,电离平衡常数减小 |
D.加入NaCN固体,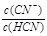 增大 增大 |
下列有关实验操作中,正确的是
| A.pH试纸在使用前先用蒸馏水润湿 | B.用酸式滴定管量取25.00 mL NaOH溶液 |
| C.容量瓶在使用前要检查是否漏水 | D.用50 mL量筒量取18.42 mL稀硫酸 |
今年菲律宾遭热带风暴“天鹰”袭击,引发大面积的洪涝灾害,灾区的饮用水需进行处理方可饮用。下列处理方式中,最合理的顺序是
①化学沉降(用明矾)②消毒杀菌(用漂粉精)③自然沉降④加热煮沸
| A.①②③④ | B.③①②④ | C.③①④② | D.①③④② |
充分燃烧7g乙烯(C2H4)气体生成CO2气体和液态H2O,放出b kJ的热量,则相同条件下乙烯燃烧的热化学方程式正确的是
| A.C2H4(g)+3O2(g) = 2CO2(g) +2H2O(l)△H = -2b kJ·mol-1 |
| B.C2H4(g)+3O2(g) = 2CO2(g) +2H2O(l)△H = +2b kJ·mol-1 |
C.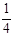 C2H4(g)+ C2H4(g)+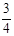 O2(g) = O2(g) =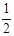 CO2(g)+ CO2(g)+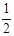 H2O(l)△H = +b kJ·mol-1 H2O(l)△H = +b kJ·mol-1 |
| D.C2H4(g)+3O2(g) = 2CO2(g) +2H2O(l)△H = -4b kJ·mol-1 |