回收利用印刷电路板上的铜制备铜的化合物,实现资源的再利用。
(1)回收利用印刷电路板上的铜制备CuCl2。
实验室模拟回收过程如下: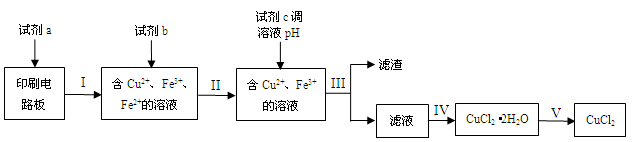
已知部分物质开始沉淀和沉淀完全时的pH如下表:
| 物质 |
开始沉淀 |
沉淀完全 |
| Fe(OH)2 |
7.6 |
9.6 |
| Fe(OH)3 |
2.7 |
3.7 |
| Cu(OH)2 |
4.4 |
8.0 |
请回答下列问题:
①步骤III的操作名称是 。
②下列试剂中,可以作为试剂a的是 。
A.HNO3溶液 B.Fe2(SO4)3溶液 C.FeCl3溶液
③若不加试剂b,直接加入试剂c调节溶液pH,是否可行? (填“是”或“否”),理由是 。
(2)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜。
已知:2H2O2(l)=2H2O (l) +O2(g) △H1=-196kJ/mol
H2O(l)=H2(g) +1/2O2(g) △H2=+286kJ/mol
Cu(s) +H2SO4(aq)=CuSO4(aq) +H2(g) △H3=+64kJ/mol
则Cu(s) +H2O2(l) +H2SO4(aq) =CuSO4(aq) +2H2O(l) △H = 。
(3)将反应Cu+H2O2+H2SO4=CuSO4+2H2O设计成原电池,其正极电极反应式是 。
(4)若用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,假设印刷电路板中其他成分不与酸反应,欲制取3mol纯净的硫酸铜,需要0.5 mol/L的硝酸溶液的体积是 L。
如图所示,已知(1)甲、乙、丁均是前三周期元素的双原子单质。(2)在一定的条件下甲与丙和甲与丁都按物质的量之比1∶3反应,分别生成X和Y,在产物中元素甲呈现负价。(3)在一定条件下乙与丙和乙与丁都按物质的量之比1∶2反应,分别生成Z和W,在产物中元素乙呈现负价。请完成下列问题: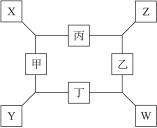
(1)甲:_________________,乙:______________。
(2)甲与丙反应生成X的反应的化学方程式:____________________________________。
(3)乙与丁反应生成W的反应的化学方程式:____________________________________。
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。已知:
①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物。
②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。
请完成下列问题:
(1)Z2Y的化学式是_______________________。
(2)Z2Y2与X2Y反应的化学方程式是_____________________。
(3)铜屑放入稀H2SO4不发生反应,若在稀H2SO4中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是_____________________________________________。
m、n、x、y四种主族元素在周期表里的相对位置如右图所示。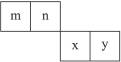
已知它们的原子序数总和为46,则:
(1)元素n的气态氢化物的化学式为__________。
(2)y的单质通入石灰乳中所生成的具有漂白性,其漂白原理是__________________(用化学方程式表示)。
(3)x的原子结构示意图为___________________________________。
(4)检验y的-1价阴离子的离子方程式为____________________________。
X、Y、Z是主族元素的单质,K、H是化合物,它们有如下关系(式中各物质的化学计量数和反应条件已略去):
(1)①X+K H+Y ②X+Z
H+Y ②X+Z H ③Y+Z
H ③Y+Z K
K
若X和Y的组成元素是同一主族,请写出符合①式的三个不同的化学方程式,并配平:___________________, __________________,__________________。
若X和Y的组成元素不是同一主族,请写出符合①式的3个不同的化学方程式,并配平(3个式子中的3种X和3种Y,分别由不同的元素组成):__________,__________,__________。
(2)今有某化合物W,它跟化合物K或CO2反应,都能生成单质Y。符合该条件(题设的3个“通式”)的单质X是__________,单质Y是__________,单质Z是__________,化合物W是__________。(均写出化学式)
已知:①A、B、C、D四种物质均含元素X,有的还可能含有元素Y、Z。元素Y、X、Z的原子序数依次递增 ②X在A、B、C、D中都不呈现它的最高化合价 ③室温下单质A与某种常见一元强碱溶液反应,可得到B和C ④化合物D受热催化分解,可制得元素Y的单质。
(1)元素X是__________________________,Z是__________________________。
(2)写出③中反应的化学方程式:_______________________________。
(3)写出④中反应的化学方程式:______________________________。