今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍。则A、B分别是
A.He和B B.C和Cl C.Na和Si D.C和Al
将一定量铁粉和铜粉的混合物加入由稀H2SO4和稀HNO3组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是
| A.反应过程中不可能产生H2 |
| B.剩余的金属粉末中一定有铜 |
| C.往反应后的溶液中加入KSCN溶液会变血红色 |
| D.往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定会减少 |
NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是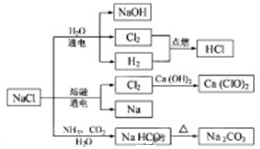
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.图中所示转化反应都是氧化还原反应 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量为世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb2S3 + 3O2 + 6Fe Sb4O6 + 6FeS②Sb4O6 + 6C
Sb4O6 + 6FeS②Sb4O6 + 6C 4Sb + 6CO↑
4Sb + 6CO↑
关于反应①、②的说法正确的是
| A.反应①②中的氧化剂分别是Sb2S3、Sb4O6 |
| B.反应①中每生成3 mol FeS时,共转移6 mol电子 |
| C.反应②说明高温下C的还原性比Sb强 |
| D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4∶3 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA |
| B.标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA |
| C.14g分子通式为CnH2n的链烃中含有的C=C的数目为NA /n |
| D.在反应KIO3 + 6HI =" KI" + 3I2 + 3H2O中,每生成3mol I2转移的电子数为6NA |
R2O8n-离子在一定条件下可把Mn2+氧化成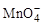 ,若反应后
,若反应后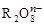 变成
变成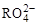 ,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为
,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为
| A.+7,2 | B.+6,2 | C.+5,1 | D.+4,1 |