下列说法正确的是
| A.形成离子键的阴阳离子间只存在静电吸引力 |
| B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
对Fe、Al2O3、SiO2、NaClO、NaAlO2的分类正确的是
| A.能与碱反应的物质是Al2O3、SiO2 | B.能与盐酸反应的物质是Fe、Al2O3、SiO2 |
| C.能与水反应的物质是Fe、Al2O3 | D.具有两性的物质是Al2O3、SiO2、NaAlO2 |
新型净水剂—高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①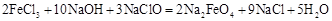
②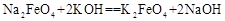 。下列说法不正确的是
。下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中氧化产物与还原产物物质的量之比为2:9 |
| C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2mol FeCl3发生反应,转移电子的物质的量为6 mol |
关于NaHCO3与Na2CO3说法正确的是
①NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火
②NaHCO3粉末中混有Na2CO3,可配置成溶液通入过量的CO2,再低温结晶得到提纯
③Ca(HCO3)2、Ba(HCO3)2、Mg(HCO3)2的溶解度都比其正盐的溶解度大,因此,NaHCO3的溶解度也应该比Na2CO3的大
④Na2CO3固体中混有NaHCO3,高温灼烧即可
⑤区别NaHCO3与Na2CO3溶液,Ca(OH)2溶液和CaCl2溶液均可用
⑥在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后,Na2CO3溶液中的红色褪去,说明BaCl2溶液具有酸性。
| A.①③ | B.③⑥ | C.②④ | D.②⑤ |
下列物质之间的转化都一步能实现的是
| A.Si→SiO2→H2SiO3→Na2SiO3 | B.Al→Al2O3→Al(OH)3→NaAlO2 |
| C.Na→NaOH→Na2CO3→NaHCO3 | D.Cu→CuO→Cu(OH)2→CuSO4 |
下列叙述不正确的是
| A.待检液逐滴加入NaOH溶液,有白色胶状沉淀产生后来沉淀逐渐消失,则原溶液中可能含有Al3+ |
| B.待检液中先加入KSCN溶液,无明显现象,再加入氯水溶液显血红色,则待检液中一定含有Fe2+ |
| C.将某化合物进行焰色实验,透过蓝色钴玻璃观察,焰色为紫色,证明含K+ |
| D.向某物质中滴加盐酸后,有能使澄清石灰水变浑浊的无色无味气体产生,证明含CO32- |