下列关于元素周期表和元素周期律的说法错误的是
| A.因为K比Na容易失去电子,所以K比Na的还原性强 |
| B.第二周期元素从Li到F,非金属性逐渐增强 |
| C.在金属和非金属的分界线处,可以找到用于作催化剂的元素 |
| D.O与S为同主族元素,且O比S的非金属性强 |
T℃时,A气体与B气体反应生成C气体. 反应过程中A、B、C浓度变化如图(Ⅰ)所示,并于t1时刻达到平衡;若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图(Ⅱ)所示. 则下列结论正确的是()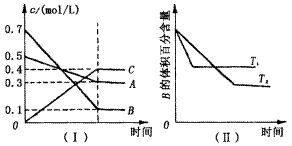
A.在(t1+10)min时,保持其它条件不变,增大压强,平衡逆向移动
B.其它条件不变,升高温度,A的转化率一定增大
C.T℃时,若由0.4mol/L A、0.4mol/L B和0.2mol/L C反应,达到平衡后,c(C)仍为0.4mol/L
D.(t1+10) min时,保持压强不变,通入稀有气体,平衡向正反应方向移动
某研究小组设想以如图所示装置用电化学原理生产硫酸。关于该装置的叙述正确的是( )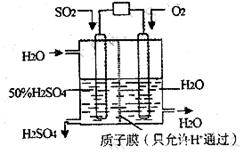
| A.该装置为电解池,通入O2的电极是阳极 |
| B.该装置中,通入SO2的电极的电极反应式为:SO2-2e-+O2-+H2O=2H++SO42- |
| C.该装置中,H+通过质子膜向左侧移动 |
| D.在标准状况下,若通人SO2速率为2.24 L·min-1,则通入O2速率应为1.12 L·min-1 |
25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是()
H++OH-;ΔH>0,下列叙述正确的是()
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
在相同温度下,等体积、等物质的量浓度的下列溶液①Na2SO4、②H2SO3、③NaHSO3、④Na2S中,所含带电微粒数由多到少的顺序为()
| A.④>①>③>② | B.①>④>③>② |
| C.①=④>②=③ | D.④=①>③>② |
已知H2(g)+I2(g) 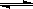 2HI(g)
2HI(g)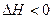 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的
有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的 平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
| A.甲、乙提高相同温度 | B.甲中加入0.1mol He,乙不改变 |
| C.甲降低温度,乙不变 | D.甲增加0.1mol H2,乙增加0.1mol I2 |