纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。
请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2+ +CO2=CaCO3↓+2NH4Cl+H2O
(2)若在实验室中进行该实验,操作l的名称是 ,该操作中用到的玻璃仪器有 (写一种即可)。
(3)上述过程制得的碳酸钙粗品表面可能含有的可溶性杂质有 (写一种溶质的化学式即可)。操作2为:洗涤粗品、检验是否已洗净、干燥固体,检验操作中选用的试剂为 (选择序号)。
①NH4Cl溶液 ②AgNO3溶液 ③CaCl2溶液 ④Ba(NO3)2溶液
(4)上述流程中的副产品可用作 。(写一种用途)
某化学小组初步探究"氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况".
实验用品:37%的浓盐酸(密度为
)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100
10%的盐酸(密度为
)
实验步骤
(1)计算:需要37%的浓盐酸的体积为
(精确到0.01
,下同);需要蒸馏水的体积为
(水的密度为
)
(2)量取浓盐酸和蒸馏水。
(3)混合配制。
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下: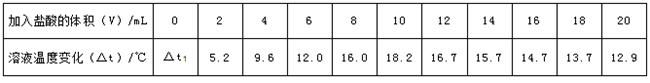
(1)表中
的值为.
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图.
(3)根据所绘曲线分析,加入盐酸的体积在0~10
时,溶液温度变化的趋势及其原因是。
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。
横坐标及猜想理由:;
纵坐标及猜想理由:。
某化学小组初步设计了"收集不同体积比例的二氧化碳和一氧化碳混合气体"的实验方案。
方案一:如图1所示
(1)请写出硬质玻璃管中发生反应的化学方程式:。
(2)该实验能获得二氧化碳和一氧化碳混合气体,其原因是。
方案二:如图2所示
请写出该气体与炭粉发生反应的化学方程式:.
方案三:如图3所示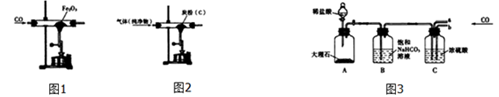
(提示:饱和
溶液的作用是除去
气体,部分夹持装置及导管已略去)
请回答下列问题:
(1)写出装置A中发生反应的化学方程式:。
(2)
气体应由(填"a"或"b")通入。
(3)写出装置C中浓硫酸的两点主要作用:
①;
②。
如图是实验室制取气体的常用装置,请回答下列问题:
(1)写出图中标号仪器的名称:①;②.
(2)实验室可加热
和
的固体混合物制取氧气,请写出该反应的化学方程式:,应选择的气体发生装置是(填字母,下同).若用向上排空气法收集氧气,验满的方法是:将放在集气瓶口,若复燃,则证明氧气已满.
(3)实验室可用
粒和稀硫酸制取氢气,请写出该反应的化学方程式:,应选择的气体发生装置是.
(4)常温下,乙烯(
)是一种无色气体,密度与空气相近,难溶于水,不与空气和水发生反应.实验室收集乙烯时,应选择的装置是.
从硅的氧化物可以制取硅单质,主要化学反应如下:
粗硅的制取:
由粗硅制纯硅(常用方法):
(1)根据上述信息,请补全制取纯硅的简易流程图:
(2)根据已有知识和上述信息,进行总结归纳:
①完成置换反应的通式:单质(I)+化合物(I)=单质(Ⅱ)+.
②填写下表: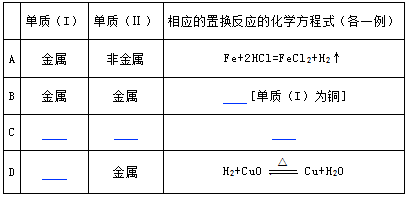
金属钠与氯气在一定条件下可以发生化学反应.
该反应的化学方程式:
.根据所给信息,请回答下列问题:
(1)当钠与氯气反应时,每个氯原子成为氯离子。
(2)从氯气变为氯化钠时,氯元素化合价的具体变化为→。
(3)氯化钠溶液能导电,是因为氯化钠溶于水形成了大量自由移动的(填微粒符号)。