发酵粉的主要成分中含有碳酸氢钠。某化学兴趣小组的同学对碳酸氢钠的性质进行了探究。
Ⅰ.定性探究
实验一:探究碳酸氢钠溶液的酸碱性
用pH试纸测得碳酸氢钠溶液的pH约为8,可知碳酸氢钠溶液呈 性。
实验二:探究碳酸氢钠的热稳定性
【查阅资料】碳酸氢钠受热容易分解,生成水、一种气体和一种常见的固体物质。
【实验1】取一定质量的碳酸氢钠放到铜片上加热,如图所示。
(1)加热一段时间后,观察到烧杯内壁有水珠。
(2)充分加热后,将烧杯迅速倒转过来,倒入适量的澄清石灰水,振荡,观察到石灰水变浑浊,说明该气体是 。
(3)欲通过进一步的实验探究来确定充分加热后的固体产物的成分。
【提出假设】①可能是Na2CO3
②可能是NaOH
③可能是 。
【实验2】
| 实验操作 |
实验现象 |
实验结论 |
| A.将该固体溶于蒸馏水配制成溶液,取少量溶液于试 管中,滴加足量稀盐酸 |
有气体产生 |
假设 (填序号)不成立 |
| B.另取少量溶液于试管中,滴加 溶液 |
|
固体产物中有 Na2CO3 |
| C.取上述B步骤静置后所得上层清液,滴入少量 溶液 |
无明显现象 |
假设①成立 |
【实验结论】NaHCO3受热分解的化学方程式为 。
【延伸拓展】实验室有两瓶失去标签的固体药品,已知它们是碳酸钠和碳酸氢钠,你能否设计一个实验进行鉴别,请简述你的实验方案及现象和结论 。。
Ⅱ.定量探究
为测定某发酵粉中碳酸氢钠的质量分数,设计了如下实验,其主要实验步骤如下:
①按下图组装仪器,取50g样品放入锥形瓶中,关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
②关闭活塞a,打开活塞b,加入足量稀硫酸溶液,直至锥形瓶内不再产生气泡;
③关闭活塞b,打开活塞a,从导管A处缓缓鼓入一定量的空气;
④测量干燥管内碱石灰(氧化钙和氢氧化钠固体的混合物)增加的质量(见上图曲线);
⑤重复步骤③和④的操作,直至干燥管内物质质量不再增加。
(1)步骤①加入样品前还应 。
(2)装置甲的作用是 ,装置乙的作用是 ;
(3)请利用相关数据计算样品中碳酸氢钠的质量分数。(写出计算过程)
达州盛产天然气,有“中国气都”之称的美誉。天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣。请你参与:提出问题:甲烷燃烧后生成哪些物质?
查阅资料:含碳元素的物质完全燃烧生成C02,不完全燃烧生成CO;无水CuS04遇水变蓝。
猜想与假设:甲:CO2 H2O;
乙:CO H2O;
丙:NH3 CO2 H2O;
丁:CO2 CO H2O。你认为__________同学的猜想是错误的,理由是________ ________ ____。
实验探究:为了验证上述猜想与假设,将甲烷在一定量的02中燃烧的产物依次通过下列装置:(无水硫酸铜能吸收水蒸气,吸水后由白色变蓝色)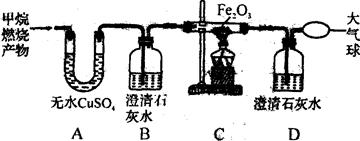
(1)A、B装置的顺序能否颠倒?(填“能”或“否”)__________________。
(2)实验中用纯净O2而不用空气的原因是_____________________________。
(3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断__________同学猜想成立。
反思与交流:为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是_______________________________。
实验室部分仪器或装置如图所示,请回答下列问题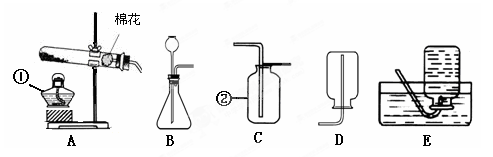
(1)写出图中标号仪器的名称:①___________ ②;
(2)写出仪器①使用时的一条注意事项。
(3)若用高锰酸钾制取并收集氧气的装置组合应选用______(填序号,下同 );
(4)实验室常用锌粒(固体)和稀硫酸(液体)制取氢气,发生装置应选用,氢气是一种难溶于水且密度比空气小的气体,所以收集氢气可以选用的装置是。
小红为大家做了一个“燃纸成铁”的趣味实验。将一张滤纸(组成元素为C、H、O)用FeCl3浓溶液润湿,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质。小红告诉大家:黑褐色物质中含有铁单质。
【提出问题】黑褐色物质中真的含有铁单质吗?
【探究过程】
(1)小红先从反应物组成分析,因为 所以反应后可能生成铁单质。
(2)为获得实验证据,小红做了实验1。
实验1:将黑褐色物质放入稀盐酸中,发现有连续微小气泡产生。若黑褐色物质中
含有铁单质,则反应的化学方程式为 。
(3)小明提出疑问:实验1中产生的气泡也可能是滤纸碳化后吸附的空气。为此,小红又做了实验2: 观察到有微小气泡产生但很快停止。
证明实验1中的连续气泡确实是由铁单质与稀盐酸反应产生的。
(4)为进一步证明黑褐色物质中有铁单质,小红又做了实验3。
实验3:将黑褐色物质放入 溶液中,观察到红色物质生成。
【得出结论】通过以上实验探究,证明黑褐色物质中确实含有铁单质。
(5)【实验反思】小红所做实验1和实验2是运用了实验,使结论更有说服力。
为检测某化工厂排放的废液中是否含有SO42-,同学们设计了如下方案,并进行了实验。
| 方案 |
步骤 |
现象 |
结论 |
| Ⅰ |
①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有SO42﹣ |
| Ⅱ |
①取样品,滴加过量_____________ ②在步骤①的溶液中滴加BaCl2溶液 |
①无明显现象 ②有白色沉淀产生 |
废液中含有SO42- |
| Ⅲ |
①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 |
①有白色沉淀产生 ②无明显现象 |
废液中含有SO42- |
(1)方案Ⅱ的实验结论如果正确,步骤①中滴加的物质是 。21世纪教育网
(2)方案Ⅰ和Ⅲ中,结论不成立的方案是 ,理由是 。
(3)方案Ⅲ的滤渣中,滴加稀硝酸是为了排除 的干扰。
在学习过程中,可以判断反应发生的方法有多种。
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL |
0 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
| 烧杯中溶液的pH |
1.1 |
1.2 |
1.4 |
1.6 |
2.0 |
7.0 |
11.0 |
12.2 |
当加入氢氧化钠溶液的体积为mL时,稀盐酸和氢氧化钠溶液恰好完全反应。
(2)在图的实验中,当观察到的现象是 就可证明NaOH与HCl发生了反应。
(3)不使用指示剂或pH试纸等方法,也可证明反应发生。向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该合理的物质是 。