(8分)
Ⅰ.醋酸是常见的弱酸。用0.1 mol•L—1NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol•L—1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH体积而变化的两条滴定曲线。
(1)滴定醋酸的曲线是 (填“I”或“Ⅱ”)。
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的溶液名称是 。
(3)V1和V2的关系:V1 V2(填“>”、“=”或“<”)
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
Ⅱ.草酸钴是制备钴的氧化物的重要原料。下图为二水合草酸钴(CoC2O4•2H2O)在空气中受热的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。
(1)通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225 ℃~300 ℃发生反应的化学方程式: 。
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比 。
(8分) 中学化学常见的物质A、B、C、D之间存在如图所示的转化关系,其中反应条件已省略。请按要求填空: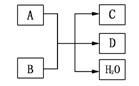
(1)若A为黑色固体单质,C、D均能使石灰水变浑浊,则该反应的化学方程式为_______________________。
(2)若A为黑色粉末,C能使品红溶液和石蕊试液褪色,则该反应的离子方程式为_____________________________________。
(3)若A为常见的碱,其溶解度随温度的升高而降低,D可作干燥剂,则C的水溶液呈____(填“酸性”、“碱性”或“中性”),其原因是________________________。
(4)若 A为红色金属单质,其质量为1.92g,与过量的B在常温下反应,用容器将全部的无色气体C收集起来,然后倒扣在水中,需通入标准状况下VmL的氧气
A为红色金属单质,其质量为1.92g,与过量的B在常温下反应,用容器将全部的无色气体C收集起来,然后倒扣在水中,需通入标准状况下VmL的氧气 恰好使C气体完全转化为B,则V=________。
恰好使C气体完全转化为B,则V=________。
红磷P(s)和Cl2(g)发生反应生成 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。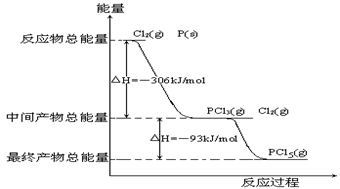
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_____________________
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出该反应的热化学方程式__________________________________________。
(2)已知H 2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
2O(l)====H2O(g);△H=+44kJ·mol-1,则16 g液态肼燃烧生成氮气和液态水时,放出的热量是________kJ。
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是________________________。
(4)已知N2(g)+2O2(g)="===2" NO2(g);△H="+67.7" kJ·mol-1, N2H4(g)+O2(g)="==" N2(g)+2H2O (g);△H=—534 kJ·mol-1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式_____________________。
已知下列反应的焓变
(1)CH3COOH(l)+2O2(g)==2CO2(g)+2H2O(l) △H1="-870.3kJ/mol"
(2)C(s)+O2(g) = =CO2(g)△H2=-393.5kJ/mol
=CO2(g)△H2=-393.5kJ/mol
(3) 2 H2(g)+O2(g) ==2H2O(l)△H3= -285.8kJ/mol 试计算反应2C(s)+2H2(g)+O2(g) ==CH3COOH(l)的焓变ΔH=
试计算反应2C(s)+2H2(g)+O2(g) ==CH3COOH(l)的焓变ΔH=
工业制氢气的一个重要反应是:CO(s)+ H2O(g) ="=" CO2(g) + H2(g)
已知25℃时:C(石墨) +O2 (g) ==CO2(g)△H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) ==CO (g)△H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g)==H2O(g)△H3=-242kJ·mol-1
试计算25℃时CO(s)+ H2O(g) ="=" CO2(g) + H2(g)的反应热_______ kJ·mol-1