25 ℃时,在20 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是
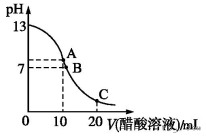
| A.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.在B点:c(OH-)=c(H+),c(Na+)= c(CH3COO-)) |
| C.在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| D.在C点: c(CH3COO-)+c(CH3COOH)=2c(Na+) |
下列属于确定有机化合物的元素组成的方法是:()
①李比希法②钠融法③铜丝燃烧法④元素分析仪法
⑤核磁共振和红外光谱法⑥质谱法
| A.①②③④ | B.②③④⑤ | C.①②⑤⑥ | D.①②③④⑤⑥ |
下列哪一个分子模型不属于比例模型:()
A.苯分子 |
B.乙醇分子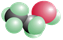 |
C.甲烷分子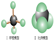 |
D.乙烯分子 |
下列说法中错误的是:()
①有机物都是从有机体中分离出来的物质②有机物都是含碳的共价化合物③有机物都不溶于水,极易溶于有机溶剂④有机物都不具备无机物的性质,都属于非电解质
| A.①③④ | B.③④ | C.②③④ | D.①②③④ |
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是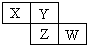
| A.X的气态氢化物比Y的稳定 |
| B.W的最高价氧化物对应水化物的酸性比Z的强 |
| C.Z的非金属性比Y的强 |
| D.X与Y形成的化合物都易溶于水 |
某些火箭和飞船升空所需的巨大能量可由下列化学反应提供:
C2H8N2 + 2N2O4 ="=" 2CO2↑ + 3N2↑ + 4H2O
有关该反应的说法正确的是
| A.该反应是分解反应 | B.反应中碳元素的化合价降低 |
| C.氧化剂是N2O4 | D.该反应不是氧化还原反应 |