X、W、Y、Z分别代表原子序数依次减小的四种短周期元素,它们满足以下条件:X原子L层电子数是其最外层电子数的2倍;W原子K、L层电子数之和比L、M层电子数之和多1个电子;Y是地壳中含量最多的元素;Z是常见的非金属元素,其一种单质能够导电。请填空:
(1)X元素在元素周期表中的位置 。原子结构示意图为 。
(2)Y和Z组成的一种其原子个数比为2:1的化合物化学式: 。
(3)W与Y可组成一种其原子个数比为1:1的化合物A,写出该化合物A的名称: ;Y和Z组成的一种化合物B,写出该化合物B与化合物A反应的化学方程式 。
工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。
某课外活动小组为了探究温度对化学平衡的影响,做了如下实验:
该小组的同学取了两个烧瓶A和B,分别加入相同浓度的NO2与N2O4的混合气体,中间用夹子夹紧,并将A和B浸入到已盛有水的两个烧杯中(如图所示),然后分别向两个烧杯中加入浓硫酸和NH4NO3固体。已知2NO2(g) N2O4(g) ΔH(298K)=-52.7kJ·mol-1。
N2O4(g) ΔH(298K)=-52.7kJ·mol-1。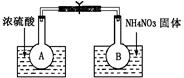
请回答:
(1)A中的现象,B中的现象 ;
(2)由此可知,降低温度,该化学平衡向(填“正”或“逆”)反应方向移动;
(3)该化学反应的浓度平衡常数表达式为,升高温度,该反应中NO2的转化率将 (填“增大”、“减小”或“不变”)。
(1)常温下,0.05mol/L硫酸溶液中,c(H+)=mol/L,pH值为,水电离的c(H+)=mol/L。如图所示,一定温度下,冰醋酸加水稀释过程中溶液的导电能力曲线图,请回答。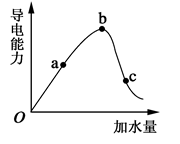
(2)“O”点为什么不导电。
(3)a、b、c三点的氢离子浓度由小到大的顺序为。
(4)a、b、c三点中,醋酸的电离程度最大的一点是。
(5)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择。
A.加NaCl溶液B.加热
C.加固体KOHD.加Zn粒
E.加固体CH3COONa F.加水
(6)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是__________________。
A.H+个数B.c(H+)
C.c(H+)/c(CH3COOH) D.CH3COOH分子数
氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2+C+N2 Si3N4+CO
Si3N4+CO
根据题意完成下列各题:
(1)配平上述化学反应方程式。
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了20mol氮气,反应生成了5mol一氧化碳,此时混合气体的平均相对分子质量是。
(3)分析反应可推测碳、氮气的氧化性:CN2(填“>”“<”“=”)。
(4)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是。
| A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
| B.在电子工业上制成耐高温的电的良导体 |
| C.研发氮化硅的全陶发动机替代同类型金属发动机 |
| D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
现有常见金属单质A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H、I,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
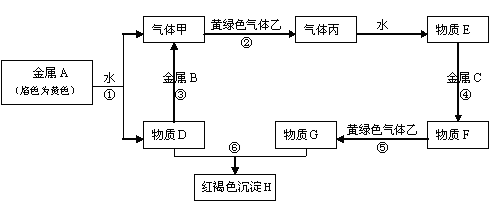
请根据以上信息回答下列问题:
⑴写出下列物质的化学式: A BF 丙
⑵写出下列反应离子方程式:
反应③
反应⑤
(3)写出反应⑧的化学方程式
(4)判断物质E是否是电解质(填“是”或“否”)