下列化学反应的离子方程式中正确的是
A.金属钠投入水中:Na+H2O Na++OH-+H2↑ Na++OH-+H2↑ |
B.漂白粉溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2 CaCO3↓+2HClO CaCO3↓+2HClO |
C.用酸性的KMnO4溶液与H2O2反应:2MnO4-+10H++3H2O2 2Mn2++3O2↑+8H2O 2Mn2++3O2↑+8H2O |
| D.用银氨溶液检验乙醛中的醛基: |
CH3CHO+2[Ag(NH3)2]++2OH- CH3COO-+NH4+ +3NH3+2Ag↓+H2O
CH3COO-+NH4+ +3NH3+2Ag↓+H2O
可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是:
2NO+O2在密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n molO2的同时生成2n molNO2②单位时间内生成n molO2的同时,生成2n molNO③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ | C.①③④ | D.①②③④⑤⑥ |
高氯酸铵(NH4ClO4)加热至483 K时,可完全分解成N2、Cl2、O2和H2O,则反应中氧化产物与还原产物的物质的量之比是
| A.1∶1 | B.1∶3 | C.2∶1 | D.3∶1 |
若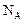 代表阿伏加德罗常数,下列说法正确的是
代表阿伏加德罗常数,下列说法正确的是
A.1 molCl2参加反应转移电子数一定为2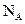 |
B.将31g的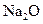 溶解于1L水中,所得溶液中 溶解于1L水中,所得溶液中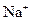 的物质的量浓度为1 mol/L 的物质的量浓度为1 mol/L |
| C.常温常压下,22.4L的NH3和16g CH4中所含有的电子数都是10NA |
D.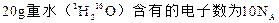 |
在下述条件下,一定能大量共存的离子组是
| A.强酸性溶液中:Al3+、K+、Mg2+、Cl-、SO42- |
| B.PH=13的溶液中:Cl-,HCO3-,NO3-,NH4+ |
| C.c(Fe3+)="0.1" mol·L-1的溶液中:Na+、SCN—、Cl-、Br- |
| D.强碱性溶液中:ClO-、SO42-、SO32-、Na+ |
下列离子方程式书写可能正确的是
| A.钠与水的反应:Na + H2O === Na+ +OH-+ H2↑ |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-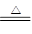 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.在氢氧化钠溶液中通入少量的CO2:2OH-+CO2=CO32-+H2O |
| D.在硫酸铝溶液中加入过量氨水:Al3+ + 4OH- = AlO2-+2H2O |