在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是 ,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量M溶液于试管中,向其中滴加 |
|
猜想①正确,碳酸钠与其反应的化学方程式为 |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH和Na2CO3;猜想二:_____;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中,滴入几滴稀盐酸 |
没有气体产生 |
“猜想一”不成立 |
他们的实验结论是否正确? ,理由是 .
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 |
实验现象 |
实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCI2溶液,B中加入 溶液 |
若A中产生白色沉淀,B中没有沉淀 |
“猜想一”成立 |
| |
“猜想二”成立 |
|
| |
“猜想三”成立 |
多角度认识物质,能帮助我们更全面了解物质世界。以碳的氧化物为例,回答下列问题:
(1)认识物质的组成和结构
二氧化碳、一氧化碳组成的相同点:;
两种物质分子构成的不同点:。
(2)认识物质的性质
①将蘸有酒精的棉芯点燃后放入烧杯,向烧杯中倾倒二氧化碳气体,观察到烧杯中的棉芯自下而上熄灭(如图1所示),说明二氧化碳具有的性质是;若使棉芯下半段立即恢复燃烧,操作方法是。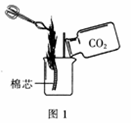
②将燃着的镁条伸入装有二氧化碳气体的烧杯中,镁条继续燃烧,说明二氧化碳还具有的性质是。
(3)认识物质的制法
某同学用软塑料瓶自制气体发生装置,通过捏放瓶身可随时控制反应发生和停止(如图2所示)。若利用该装置制取二氧化碳,反应的化学方程式;若实验利用该装置制取氧气无纺布包内药品为(写化学式)
(4)认识物质的用途
①扬其利抑其弊。减少二氧化碳排放以控制温室效应,合理使用二氧化碳为人类造福。请举二氧化碳用途一例:。
②控制条件获取所需物质。反应物相同,条件不同,产物不同。请举一例:。
科学探究是奇妙的过程,再一次实验中小文不小心把硫酸铁溶液滴加到了盛有5%H 2 O 2 的溶液的试管中,立即有大量的气泡产生.硫酸铁溶液中含有三种粒子(H2O、SO42-、Fe3+),小文想知道硫酸铁溶液中的哪种粒子能使双氧水分解的速率加快.请你和小文一起通过下图所示的三个实验完成这次探究活动,并填写空白.
(1)你认为最不可能的是哪一种粒子________,理由是.
(2)检验实验产生的气体是否是氧气的方法是.
(3)在实验②中加入稀硫酸后,无明显变化,说明________不起催化作用;
(4)小明如果要确定硫酸铁是催化剂,还须通过实验确认它在化学反应前后______________.
(5)经证明硫酸铁是过氧化氢分解的催化剂,写出硫酸铁催化过氧化氢分解的化学方程式____________.
注意:若答对(6)小题奖励4分,但化学试卷总分不超过60分。
(6)小华通过实验发现,硫酸铁溶液的浓度也会影响过氧化氢分解的速率,常温下,他在a,b,c,三个试管中分别加入等量5%过氧化氢的溶液,在其他条件相同时,各滴2滴5%、10%、20%的硫酸铁溶液。根据实验数据绘制了产生的氧气体积和时间变化的曲线如图。请你观察右图回答问题。
①写出两条规律性结论:____________。
②若实验中所得的曲线如图中虚线所示,请推测其中可能的原因____________。
食品包装袋中常用脱氧剂。某化学兴趣小组将脱氧剂封口打开,将其倒在滤纸上,
观察到脱氧剂大部分为黑色粉末,其中还夹杂着少量红色粉末。
【提出问题】该脱氧剂中的黑色、红色粉末各是什么?
【提出猜想】黑色粉末可能含炭粉、铁粉、氧化铜中的一种或几种。红色粉末可能含有氧
化铁、铜粉中的一种或几种。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
取脱氧剂粉末加入足量稀硫酸 |
粉末几乎全部溶解,只有少量黑色粉末未溶解,有气泡产生,溶液变成黄色 |
| ② |
去实验①的残渣灼烧,将内壁有澄清石灰水的小烧杯罩在上方 |
澄清石灰水变浑浊 |
【得出结论】由实验①②可知,脱氧剂中黑色粉末肯定含。
脱氧剂中的红色粉末肯定不含,肯定含,写出相应的化学方程式。
【拓展延伸】小明认为铁生锈时会消耗氧气,因此可用此脱氧剂(实验室可滴几滴水)测定空气中氧气的含量,装置如图所示。集气瓶的实际容积是150mL,量筒内盛100mL的水。当量筒内水面不再变化,且温度恢复至室温时,读出水面在73mL刻度处。由上述实验数据可以算出,空气中氧气的体积分数是。本实验的测量结果与理论值不一致,原因可是。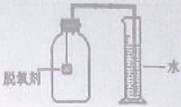
粗盐中含有泥沙等难溶性杂质和氯化镁、氯化钙等可溶性杂质,某学习小组做粗盐的提纯实验。
【提出问题】如何才能将粗盐中的杂质除去,获得精盐?
【实验方案】该小组按以下流程进行实验。
【问题讨论】
(1)实验步骤②③④都需要进行操作,该操作中玻璃棒的作用是。
(2)沉淀X是,沉淀Y是。
(3)有同学认为该实验方案不完善,请你说明原因并补充完善:。
(4)将实验所得的精盐在烧杯中配制成100g 8﹪的氯化钠溶液。经检测,所配溶液溶质质量分数偏小,其可能原因有(填序号)。
①精盐称量时,仅在左盘垫上了称量纸,而右盘没有垫上称量纸;
②溶解时所用烧杯不干燥;
③所得精盐未完全干燥。
(5)工业上用电解饱和食盐水的方法可制取氢氧化钠,同时还生成两种气体单质。写出此反应的化学方程式。
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究。
【查阅资料】①通常情况下,1体积水溶解1体积的CO2。
②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生。
【实验探究】小红同学设计了下图所示的实验装置(锥形瓶内充满CO2),并进行实验。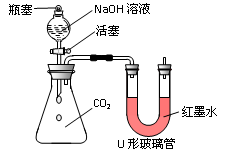
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面______(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是___________。请根据初中化学知识写出CO2与NaOH溶液反应的化学方程式:____________。
【反思与评价1】小明认为小红的实验方案不严密,理由是_______________________。
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究。请填写表中的空格。
| 实验方法 |
操作过程 |
现象 |
实验结论 |
| 方法一 |
取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液 |
有白色沉淀生成 |
CO2与NaOH发生了反应 |
| 方法二 |
取小红实验后锥形瓶内的溶液适量,加入足量稀硫酸 |
______________ |
【反思与评价2】同学们经过讨论,认为【拓展实验】的______(填“方法一”或“方法二”)依然不严密,理由是___________________________(用化学方程式表示)。