下列分离或除杂方法不正确的是
| A.用蒸馏法分离水和酒精 |
| B.用萃取法分离苯和溴苯 |
| C.用重结晶法除去硝酸钾中的氯化钠杂质 |
| D.用饱和NaHCO3溶液除去CO2中混有的少量HCl气体 |
进行中和滴定时,事先不应用所盛装溶液润洗的仪器是()
| A.酸式滴定管 | B.锥形瓶 |
| C.量筒 | D.碱式滴定管 |
下列装置或操作能达到预期实验目的的是()
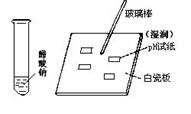
测定中和热测定2mol/L醋酸钠溶液PH
A B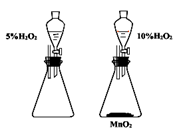

研究催化剂对反应速率的影响探究弱酸酸性相对强弱
CD
常温下,将VL0.10mol·L-1盐酸和VL0.06mol·L-1Ba(OH)2溶液混合后,该混合液的pH为(设混合后总体积为2VL)()
| A.1.7 | B.2 | C.12 | D.12.3 |
能说明醋酸是弱电解质的是()
①用浓硫酸和醋酸钠固体共热可制得醋酸 ②醋酸钠溶液呈碱性
③可以用食醋清除热水瓶内的水垢 ④pH=2醋酸溶液稀释1000倍后pH小于5
| A.② | B.①② | C.②④ | D.①③④ |
已知反应a W(g)= b Z(g)的△H < 0、△S > 0,对此反应叙述正确的是()
| A.该反应在任何情况下均能自发进行 |
| B.该反应在任何情况下均不能自发进行 |
| C.该反应在一定条件下能自发进行 |
| D.条件不足,无法判断 |