PM2.5是连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤.机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
(1)将PM2.5样本用蒸馏水处理制成待测试样。测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 |
K+ |
Na+ |
NH4+ |
SO42- |
NO3- |
Cl- |
| 浓度/mol•L-1 |
4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据判断PM2.5试样的pH 。
(2)汽车尾气的排放是城市重要的污染源,尾气含有的NO会破坏臭氧层。利用催化技术可将尾气中的NO和CO转变成CO2和N2,其反应方程式为:2NO+2CO=CO2+N2.为探究某种催化剂对反应速率的影响,t℃时,用气体传感器测得不同时间的NO和CO浓度如表:
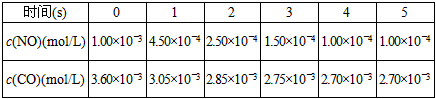
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
①在上述条件下反应能够自发进行,则反应的△H___________0(填写“>”、“<”、“=”)。
②前2s内的平均反应速率v(N2)=______________。
③在该温度下,反应的平衡常数K=________________。
④假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
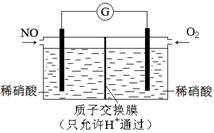
(3)某化学兴趣小组构想将NO转化为HNO3,装置如下图,电极为多孔惰性材料。则负极的电极反应式是 。
聚甲基丙烯酸酯纤维具有质轻、频率宽等特性,广泛应用于制作光导纤维。已知A为某种聚甲基丙烯酸酯纤维的单体,其转化关系如下: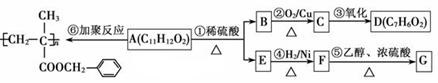
(1)A的结构简式为 。
(2)下列有关E的说法不正确的是 (填写字母编号)
| A.能使酸性高锰酸钾溶液褪色 | B.能使溴的CCl4溶液褪色 |
| C.一定条件下,能够发生消去反应 | D.一定条件下,能够发生取代反应 |
(3)F的同分异构体中属于酯类的有 种
(4)反应②的化学方程式是
反应⑤的化学方程式是
按要求完成下列问题:
(1) 系统命名为 ;
系统命名为 ;
(2)4―甲基―1―戊烯的键线式为 。
(3)写出乙醛与新制氢氧化铜反应化学方程式;
(4)丙三醇与硝酸反应能生成三硝酸甘油酯,写出三硝酸甘油酯的结构简式
(5)下列有关实验的说法不正确的是_____________。
| A.制乙烯时,温度计应插入反应混合液中 |
| B.实验室用溴和苯在铁粉存在下反应,得到的溴苯显褐色,原因是溴苯在空气中被氧化 |
| C.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液 |
| D.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤 |
E.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少
桂醛在食品、医药、化工等方面都有应用。肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
(1)肉桂醛由C、H、O三种元素组成,质谱分析肉桂醛分子的相对分子质量为132,其分子中碳元素的质量分数为81.8%,肉桂醛的分子式是 。
肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原子,其结构简式是。(不考虑顺反异构与对映异构)
(2)已知:
I.醛与醛能发生反应,原理如下: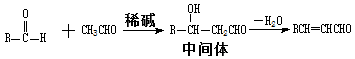
II.合成肉桂醛的工业流程如下图所示,其中甲为某种烃。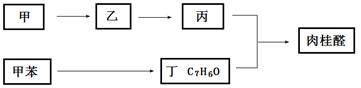
①甲的结构简式是。
②丙和丁生成肉桂的化学方程式是。
(3)肉桂醛能被银氨溶液氧化,再经酸化得到肉桂酸,写出肉桂酸甲酯的结构简式。
(4)现用芳香烃A为原料合成肉桂酸甲酯H的路线如下,测出A的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰2︰1︰2。: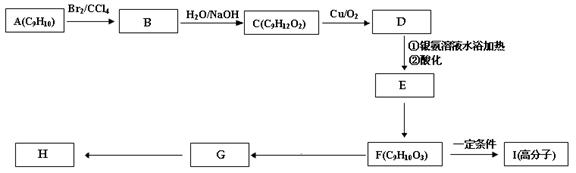
①化合物F中的官能团有 (填名称)。
②B→C的反应类型是 ,F→G的反应类型是 ,
③书写化学方程式
F→I
G→H
④G的同分异构体中,属于酯类目苯环上只有一个取代基的同分异构体有种。
其结构简式分别是
(1) 用系统命法写出下列物质名称或结构简式
2,2,3-三甲基丁烷的结构简式是
画出3-甲基-1-丁烯的键线式。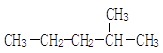 的系统命名是:
的系统命名是:
(2)写出下列反应的化学方程式
苯的硝化反应
乙烯发生加聚反应
乙醛与新制氢氧化铜反应
(1)下列各组化合物中,属于同系物的是(填入编号),属于同分异构体的是(填入编号)。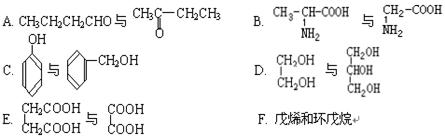
(2)有机物A: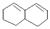 在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
方程式
(3)某高分子有机物 是由一种单体缩聚而成的,该单体的结构简式为。
是由一种单体缩聚而成的,该单体的结构简式为。