下列物质性质与应用对应关系正确的是
| A.浓硫酸具有吸水性,可用于干燥CO2 |
| B.工业上用焦炭还原二氧化硅制取晶体硅,同时生成二氧化碳 |
| C.氢氧化铁溶胶、NaCl溶液、淀粉溶液均具有丁达尔效应 |
| D.金属铁和铝为生活中常用的金属材料,因为铝的活泼性大于铁,所以通常状况下,铝比铁更容易锈蚀 |
化合物A的分子式为C4H9NO2,A的同分异构体中属于氨基酸的有
| A.5种 | B.4种 | C.3种 | D.6种 |
化合物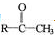 与NaOH溶液、碘水三者混合可发生如下反应:
与NaOH溶液、碘水三者混合可发生如下反应:
(1)I2+2NaOH═NaI+NaIO+H2O
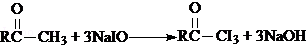
(2)
(3)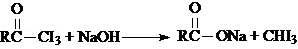
此反应称为碘仿反应.根据上述反应方程式,推断下列物质中能发生碘仿反应的是
| A.CH3CHO | B.CH3CH2CHO | C.CH3CH2COCH2CH3 | D.CH3COCH2CH3 |
下列各组中的两种有机物,其最简式相同但既不是同系物,又不是同分异构体的是
| A. |
苯苯乙烯 |
B. |
甲醛乙二醛 |
C. |
乙烯丙烯 |
D. |
甲酸乙醛 |
已知酸性大小:羧酸>碳酸>酚>HCO3﹣.下列含溴化合物中的溴原子,在适当条件下都能被羟基(﹣OH)取代(均可称之为水解反应),所得产物能跟NaHCO3溶液反应的是
| A. |
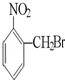 |
B. |
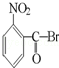 |
C. |
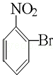 |
D. |
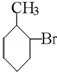 |
已知戊烷有3种同分异构体,可以被催化氧化成醛的戊醇的同分异构体(属醇类)的数目有
| A.4种 | B.5种 | C.7种 | D.8种 |