(18分) 完成下列空白。
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,下图是异辛烷的球棍模型,则异辛烷的系统命名为_________ ___ _。
(2)写出下列反应的化学方程式
①2,5-二甲基-2,4-己二烯与足量氢气加成: ;
②2-甲基-2-丁烯加聚反应_______________ __
③甲苯在一定条件下生成三硝基甲苯:________________________________
④实验室制备乙烯:________________________________
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr → CH3CHBrCH3+CH3CH2CH2Br
(主要产物) (次要产物)
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,且B中仅含有4个碳原子、1个溴原子、1种氢原子。则B的结构简式为 ,A的结构简式为
下列各组物质属于同系物的是,属于同分异物体的是;属于同位素的是 ,属于同素异形体的是,属于同一种物质的是。(填序号)
⑴O2和O3⑵氕和氚 ⑶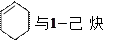 ⑷苯和对二甲苯
⑷苯和对二甲苯
⑸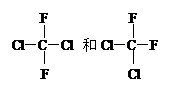 ⑹
⑹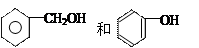 ⑺
⑺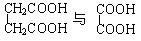
⑻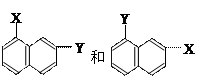 ⑼
⑼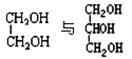 (10) 乙醇和乙醚
(10) 乙醇和乙醚
如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空: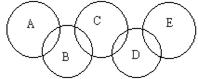
(1)写出下列物质的化学式:A ,B ,D 。
(2)写出下列反应的离子方程式:B+C: ,
,
(3)相连环物质间发生的反应中,氧化还原反应共有个。
有A、B、C、D四种无色溶液,它们分别是Na2CO3、Na2S O4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为:①A+D→溶液+气体,②B+C→溶液+沉淀,③B+A→溶液+沉淀X,④D+B→溶液Y+沉淀,⑤溶液Y+沉淀X→溶液+气体。
O4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为:①A+D→溶液+气体,②B+C→溶液+沉淀,③B+A→溶液+沉淀X,④D+B→溶液Y+沉淀,⑤溶液Y+沉淀X→溶液+气体。
(1)根据以上记录确定:A_____________B____________C_______________D______________(填化学式)
(2)写出①、⑤各反应的离子方程式:
①
⑤
(1)两个同容积的密封容器A、B,常温下,A中充入a g A气体,B中充入a g CH4气体,A与B内的压强之比是4∶11,则A的摩尔质量为_________________。
(2)某氯化镁溶液的密度为d g/cm3,其中镁离子的质量分数为w,a mL该溶液中Cl-
的物质的量为。
(3)标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ mL),所得溶液的密度为ρ g/ mL, 则该溶液的溶质的物质的量浓度为。
(4)在 11P + 15 CuSO4 +24 H2O =" 5" Cu3P +6 H3PO4 +15 H2SO4中,每 1 mol CuSO4可以氧化磷的物质的量是 __________ 。
、氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为(用a、b 表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为  。
。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续
不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ. 2Li + H2 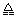 2LiHⅡ. LiH + H2O ="=" LiOH + H2↑
2LiHⅡ. LiH + H2O ="=" LiOH + H2↑
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度约为0.8g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。