用软锰矿(主要成分为MnO2)生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如下图: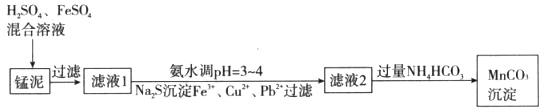
(1)锰泥中加入H2SO4、FeSO4混合溶液,反应的离子方程式是__________。
(2)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中c(H+)/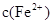 <0.7时,滤液1中能够检验出有Fe
<0.7时,滤液1中能够检验出有Fe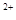 ;
;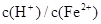 ≥0.7时,滤液1中不能检验出有Fe2+。
≥0.7时,滤液1中不能检验出有Fe2+。
①检验Fe2+是否氧化完全的实验操作是__________。
②生产时H2SO4、FeSO4混合溶液中c(H+)/c(Fe2+)控制在0.7~1之间,不宜过大,请从节约药品的角度分析,原因是__________。
若c(H+)/c(Fe2+)>1,调节c(H+)/c(Fe2+)到0.7~1的方法是__________。
(3)写出滤液2中加入过量NH4HCO3反应的离子方程式__________。
(4)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3__________kg(已知相对分子质量:MnO2 87;MnCO3 115)。
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)△H= ―47.2kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
氮是地球上含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用。
(1)下图是1mol NO2气体和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2气体和CO反应的热化学方程式:。
(2)已知: CO(g)+1/2 O2(g)= CO2(g) △H = -283 kJ/mol
N2(g)+ O2(g) ="" 2 NO(g)△H = +180 kJ/mol
则反应2 NO(g)+2 CO(g) N2(g) + 2 CO2(g) △H =kJ/mol。
N2(g) + 2 CO2(g) △H =kJ/mol。
(3)在固定体积的密闭容器中,进行如下化学反应: N2(g)+3H2(g) 2NH3(g);△H<0,其平衡常数K与温度T的关系如下表:
2NH3(g);△H<0,其平衡常数K与温度T的关系如下表:
| T/K |
298 |
398 |
498 |
| 平衡常数K |
4.1×106 |
K1 |
K2 |
①写出该反应的平衡常数表达式:K =
②试判断K1K2(填写“>”“=”或“<”)
③下列各项能说明该反应一定达到平衡状态的是(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(H2)(逆) =)3v(N2)(正)
c.容器内压强保持不变 d.混合气体的密度保持不变
④若上述反应达到平衡时,N2、H2、NH3的浓度之比为1:3:2,再向容器中按物质的量之比为1:3:2通入N2、H2、NH3,与原平衡相比,N2的物质的量浓度(填增大、不变或减小,下同),NH3的体积分数。
已知:A为酸式盐,B为某二价主族金属元素的化合物,其中B的化学式中共有32个电子, 常温常压下C、D、F、G、I均呈气态 ,除G呈红棕色外其他气体均为无色。等物质的量A、B与少量的水充分混合能恰好完全反应。图中反应条件(除高温外)均已略去。
(2)写出A与B反应的化学方程式。
(3)写出下列反应的离子方程式:
①在A溶液中加入M
②向A溶液中加入过量NaOH溶液,并加热
(4)C还可在纯氧中安静燃烧,产物为H和一种单质,写出该反应的化学方程式:
A、B、C、X均为中学化学中常见的纯净物,它们之间有如图所示的转化关系(副产物已略去)。
试回答:
(1)若X是强氧化性单质,则A可能是。(填序号)
a、S b、Na c、Mg d、Al
(2)若X为金属单质,向C的溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为;C溶液在储存时应加入少量X,理由是(用离子方程式表示)。
(3)若A、B、C为含同种金属元素的无机化合物,X为强酸或强碱。A和C在H2O溶液中反应生成B的离子方程式为。
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条
件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与Y、Z、W可组成化学式为YX3、X2Z和X2W三种共价化合物。请填空:
(1)X、Y、Z原子最外层电子数之和是;
(2)X2W的电子式是 ,YX3、X2Z和X2W形成的晶体类型都属于;
(3)X、Y和Z组成的一种化合物是强酸。写出该酸的稀溶液与铜反应的离子方程式;X、Y和Z组成的另一种化合物是离子化合物,该离子化合物在210℃分解生成一种只含Y、Z的气体和一种只含X、Z的液体(在常温、常压下)。已知40g该离子化合物完全分解可生成11.2L的气体(标准状况下),该气体的化学式为:;
(4)X、Y、Z和W组成一种化合物,其原子个数之比为5:1:3:1;该化合物具有还原性。
①写出该化合物与过量稀NaOH溶液反应的离子方程式:。
②请设计实验证明该化合物具有还原性:
。