[化学——选修2:化学与技术]水是一种重要的自然资源,是人类赖以生存不可缺少的物质,水质优劣直接影响人体健康。请回答下列问题:
(1)某贫困山区,为了寻找合适的饮用水,对山上的泉水进行了分析化验,结果显示,水中主要含Ca2+、Mg2+、Cl-和SO42-。则该硬水属于________(填“暂时”或“永久”)硬度,若要除去Ca2+、Mg2+,可以往水中加入石灰和纯碱,试剂加入时先加________后加________。
(2)我国规定饮用水的硬度不能超过25度。硬度的表示方法是:将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把1升水中含有10 mg CaO称为1度。某化学实验小组对本地区地下水的硬度进行检测。
实验中涉及的部分反应:
M2+(金属离子)+EBT-(铬黑T)===MEBT+
蓝色 酒红色
M2+(金属离子)+Y4-(EDTA)===MY2-
MEBT++Y4-(EDTA)===MY2-+EBT-(铬黑T)
实验过程:
①取地下水样品25.00 mL进行预处理。写出由Mg2+引起的暂时硬度的水用加热方法处理时所发生反应的化学方程式:_______________________________________。
②预处理的方法是向水样中加入浓盐酸,煮沸几分钟,煮沸的目的是_______________________。
③将处理后的水样转移到250 mL的锥形瓶中,加入氨水—氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.010 00 mol·L-1的EDTA标准溶液进行滴定。滴定终点时共消耗EDTA溶液15.00 mL,则该地下水的硬度为______________。
(3)某工业废水中含有CN-和Cr2O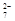 等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理: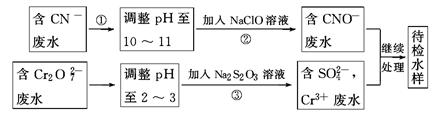
回答下列问题:
①流程②中,反应后无气体放出,该反应的离子方程式为_______。
②含Cr3+废水需进一步处理,请你设计一个处理方案:_______。
Ⅰ.由于温室效应和资源短缺等问题,如何降低大气中的 CO2含量并加以开发利用, 引起了各国的普遍重视。工业上有一种方法是用 CO2生产燃料甲醇。一 定条件下发生反应:CO2(g) +3H2(g) CH3OH(g)+H2O(g)。右图表示该 反应进行过程中能量(单位为 kJ•mol -1)的变化。
(1) 为探究反应原理,现进行如下实验:T1℃时,在体积为 1L 的密闭容器中,充入 1mol CO2和 3mol H2,测得CO2和 CH3OH(g) 的浓度随时间变化如 图所示。从反应开始到平衡,用氢气浓度变化表示的平均反应速率 v(H2)为mol•L-1•min-1。
(2)温度变为 T2℃(T1 > T2),平衡常数 K (填“增大”、 “不变”或“减小”)。
(3)下列措施中能使 n(CH3OH)/n(CO2)增大的有
A升高温度 B加入催化剂 C将 H2O(g)从体系中分离
D再充入 1molCO2和 3molH2 E.充入 He(g),使体系总压强增大。
Ⅱ.在温度 t℃,某 NaOH 的稀溶液中 c(H+)=10—amol/L,c(OH—)=10—bmol/L,已知 a+b=12,该温度下水的离子积 Kw= ;t 25℃(填“大于”、“小于”或“等于”)。
向该溶液中逐滴加 pH=c的盐酸(t℃),测得混合溶液的部分 pH 如右表 所示。假设溶液混合前后的体积变化 忽略不计,则 c 为
(共8分)A、B、C、D、E均为可溶于水的固体,组成他们的离子有
| 阳离子 |
Na+ Mg2+ Al3+ Ba2+ |
| 阴离子 |
OH- Cl- CO32- SO42- HSO4- |
分别取它们的水溶液进行实验,结果如下:①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
(1)据此推断它们是(写化学式)A ;B ;C ;D ;E 。
(2)写出④中反应的离子方程式:。
(3) A溶液中各种离子浓度由大到小的顺序为。
实验室用Na2SO3固体与70%的硫酸反应制取SO2气体时,可用NaOH溶液或Fe2(SO4)3溶液吸收多余的SO2气体。
(1)用NaOH溶液吸收多余的SO2气体,若两者恰好反应生成Na2SO3溶液,则Na2SO3溶液中各微粒间浓度关系正确的是_______。
| A.c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+) |
| B.c(Na+)=2c(SO32-) + 2c(HSO3-) + 2c(H2SO3) |
| C.c(Na+) + c(H+)=2c(SO32-) + c(HSO3-) + c(OH-) |
| D.c(H+) + c(HSO3-) + 2c(H2SO3)=c(OH-) |
(2)用Fe2(SO4)3溶液吸收多余的SO2气体,写出SO2与Fe2(SO4)3溶液反应的离子方程式__________
(3)用Fe2(SO4)3溶液吸收SO2气体一段时间后,吸收液中一定存在的离子有H+、Fe2+、SO42-和极少量的OH-。某同学认为还可能存在其他离子,并提出假设进行实验探究。
①提出合理假设:
假设1:还存在HSO3-、SO32-;
假设2:还存在Fe3+;
假设3:___________________
……
②设计实验方案
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量吸收液于试管中,加稀硫酸酸化,然后再滴入几滴品红溶液; |
现象:________________________________ 结论:假设1不成立; |
| 步骤2:______________________________ ____________________________________。 |
现象:________________________________ 结论:假设2成立。 |
含碳化合物在国民经济中占有重要地位。含碳化合物的性质、制备等一直是中学化学研究的焦点。
研究情境一:工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯 △H=-166kJ·mol-1,平衡常数K
△H=-166kJ·mol-1,平衡常数K
其中乙苯在CO2气氛中的反应可分两步进行。
第一步: ΔH1,平衡常数K1
ΔH1,平衡常数K1
第二步:H2(g) +CO2(g) CO(g) + H2O(g) ΔH2=-41kJ·mol-1,平衡常数K2
CO(g) + H2O(g) ΔH2=-41kJ·mol-1,平衡常数K2
(1)上述第一步反应的ΔH1=____________,K、K1、K2之间的关系是________________。
(2)某化学研究性学习小组模拟工业用乙苯与CO2脱氢生产苯乙烯。在3L固定容积密闭容器内,乙苯与CO2的反应在I、II、III三种不同的条件下进行实验。乙苯、CO2的起始浓度分别为1.0mol·L-1和3.0mol·L-1,其中实验I在T1°C,0.3MPa,而实验II、III分别改变了实验其他条件。乙苯的浓度随时间的变化如图所示。
①实验I 苯乙烯在0—50min的平均反应速率是____________。
②实验III改变的条件可能是_______________________________________________。
③对于实验I,下列叙述能说明乙苯与CO2反应达到平衡的是_______。
a.平衡常数K不再增大b.CO2的转化率不再增大
c.混合气体的平均相对分子质量不再改变 d.反应物不再转化为生成物
研究情境二:2013年12月14日21时11分,嫦娥三号探测器在月球表面预选着陆区域成功着陆,标志我国已成为世界上第三个实现地外天体软着陆的国家。
(3)下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液。
如果某段时间内氢氧储罐中共收集到67.2L气体(标准状况),则该段时间内水电解系统中转移电子的物质的量是________mol。
(4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO + O2,同时生成的CO可用作燃料。已知该反应的阳极反应是:
4OH--4e-=O2↑+2H2O,则阴极反应是__________________。
(14分) CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
| 物质 |
开始沉淀 |
沉淀完全 |
| Fe(OH)3 |
2.7 |
3.7 |
| Cu(OH)2 |
5.6 |
6.7 |
| Al(OH)3 |
3.8 |
4.7 |
已知:CuCl溶于NaCl的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释后可生成CuCl沉淀。
(1)煅烧的主要目的是:。
(2)操作Ⅰ为调节溶液的PH值,范围为,加入的物质X可以是()
A、CuO B、Cu(OH)2 C、NaOH 溶液 D、CaCO3
(3)滤渣Ⅱ的主要成分是。
(4)往滤液Ⅱ中加入食盐并通入SO2可生成CuCl2-,请写出反应的离子方程式:。
(5)在反应Ⅰ中,温度控制在70~80℃并使用浓NaCl溶液,主要目的是:。
(6)常温下,已知CuOH的KSP为1.0×10-14,则Cu++H2O  CuOH + H+的平衡常数为:。
CuOH + H+的平衡常数为:。