在容积为2 L的恒容密闭容器中,一定温度下,发生反应:aM(g)+bN(g) cQ(g),正反应放热。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述错误的是
cQ(g),正反应放热。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述错误的是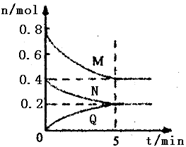
| A.该温度下此反应的平衡常数的值K=25 |
| B.若条件改为恒温恒压,则达平衡时M的转化率小于50% |
| C.相同条件下,若开始时向容器中充入0.4molQ,达到平衡时,M的体积分数等于50% |
| D.若条件改为绝热,则达平衡所需时间更短 |
下列化工生产过程中,不涉及化学变化的是
| A.硫酸厂用接触法生产硫酸 | B.炼铁厂用热还原法冶炼铁 |
| C.氮肥厂用氢气和氮气合成氨气 | D.炼油厂用分馏法生产汽油 |
一定条件下,中学化学常见物质甲、乙之间存在如下转化关系,则乙不可能是
| A.H2SiO3 | B.Fe(OH)3 | C.NH4Cl | D.NO2 |
镁—过氧化氢燃料电池具有比能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4==MgSO4+2H2O,结构示意图如图所示。下列关于该电池的叙述正确的是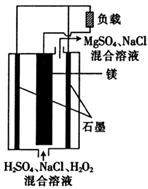
| A.想要实现该反应,电池内部可以使用MnO2作填料 |
| B.电流工作时,H+向Mg电极移动 |
| C.电池工作时,正极的电极反应式为Mg—2e-==Mg2+ |
| D.电池工作时,电解质溶液的pH将不断变大 |
下列热化学方程式中的△H能正确表示物质的燃烧热的是
| A.CO(g)+1/2O2(g) = CO2(g)△H =-283.0 kJ/mol |
| B.C(s) +1/2O2(g) = CO(g)△H =-110.5 kJ/mol |
| C.H2(g) +1/2O2(g) = H2O(g)△H =-241.8 kJ/mol |
| D.2C8H18(l) +25O2(g) = 16CO2(g)+18H2O(l)△H =-11036 kJ/mol |
已知:2Zn(s)+O2(g)=2ZnO(s)△H =-701.0 kJ/mol ①
2Hg(l)+O2(g)=2HgO(s)△H =-181.6 kJ/mol②
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的△H为
| A.+519.4 kJ/mol | B.+259.7 kJ/mol |
| C.-259.7 kJ/mol | D.-519.4 kJ/mol |