某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上。某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在。所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3·H2O。
背景资料:
①锌与铝性质相似,可以与NaOH溶液反应生成H2和Na2ZnO2;
②Zn(OH)2为白色固体,难溶于水,可溶于强碱和氨水。与氨水反应生成配合物[Zn(NH3)4]2+,该配合物遇强酸反应生成Zn2+、NH4+
甲同学设计的实验方案如下:

(1)方案中试剂M是 ;沉淀A是 。
(2)操作Ⅰ的主要过程是:在滤液中逐滴加入 ,直至生成的沉淀刚好溶解,再加入足量的 。
(3)若金属中含铝,则沉淀 (选填沉淀编号)的质量不为零;若金属中含锌,则沉淀 (选填沉淀编号)的质量不为零。若沉淀B、C的质量均不为零,则生成B的离子方程式为: 。
(4)乙同学对甲同学的方案做了如下改进:

沉淀D为 ,与甲同学的方案相比,此方案的优点 。
(5)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图像正确的是 。

(6)上题中当沉淀质量最大时,溶液呈 (从下列选项中选填,下同);当沉淀只有一种成分时,溶液可能呈 。
A.酸性 B.中性
C.碱性 D.可能酸性,也可能碱性
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题: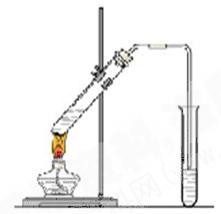
(1)写出制取乙酸乙酯的化学反应方程式。
(2)浓硫酸的作用是。
(3)饱和碳酸钠溶液的主要作用是
。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
防止 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:
苯甲醛易被空气氧化;苯甲醇的沸点为205.3℃;苯甲酸的熔点121.7℃,沸点249℃,溶解度0.34g(常温);乙醚的沸点34.8℃,难溶于水。
制备苯甲醇和苯甲酸的主要过程如下:
(1)混合苯甲醛、氢氧化钾和水应选用的仪器是 (填序号)。
(填序号)。
A.带胶塞的锥形瓶 B.烧杯
C.容量瓶
(2)操作I的名称是 。
。
(3)操作II的名称是,产品甲的成分是。
(4)操作III的名称是,产品乙是。
(5)在使用下图所示的仪器的操作中,温度计水银球x的放置位置为(填图标a、b、c、d)。控制蒸气的温度为。
某学生活动小组设计了溴苯的制取装置,如图所示。请填写下列空白: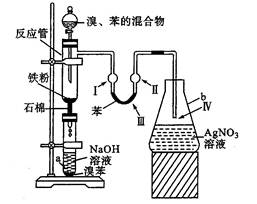
(1)制取溴苯的反应方程式是:
。
(2)在滴入混合液几分钟后,能观察到的现象是:
Ⅰ处:,
Ⅱ处:,
Ⅲ处:,
Ⅳ处:。
(3)在2~3min后,可以在a管底部得到。
(4)NaOH的作用是,
U形管中苯的作用是,
AgNO3 溶液的作用是。
某实验小组同学对电化学原理进行了一系列探究活动。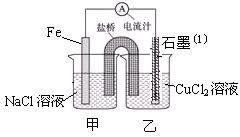
(1)右图为某实验小组依据氧化还原反应:(用离子方程式表示)设计的原电池装置,一段时间后,两电极质量相差12g,导线中通过mol电子。
(2)其它条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为,这是由于NH4Cl溶液显性,(填酸性、碱性或中性)用离子方程式表示溶液显此性的原因,用吸管吸出铁片附近溶液少许至于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是,电极反应为;乙装置中石墨(1)为极(填正、负、阴、阳),乙装置中与铜线相连石墨电极上发生的反应式为,产物常用检验,反应的离子方程式为。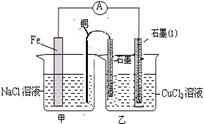
为比较Fe2+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题: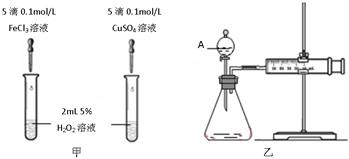
(1)定性分析:如图甲可通过观察定性比较得出结论,有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为,实验中需要测量的是。
(3)某同学要利用乙装置测定某H2O2溶液的物质的量浓度。在锥形瓶中加入0.10 mol MnO2粉末后加入50 mL 该H2O2溶液,在标准状况下放出气体的体积和时间的关系如图所示。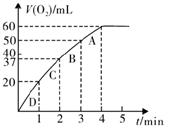
①写出H2O2在MnO2作用下发生反应的化学方程式;
②实验中放出气体的总体积是mL;
③A、B、C、D各点反应速率快慢的顺序为>>>;
④计算H2O2的初始的物质的量浓度。(结果保留2位小数)